Διαγνωστικά και θεραπευτικά πρωτόκολλα οστεοπόρωσης κατά τον ΕΟΦ
Η οστεοπόρωση είναι μια συχνή νόσος, η οποία χαρακτηρίζεται από χαμηλή οστική μάζα, διαταραχή της μικροαρχιτεκτονικής του οστού, σκελετική ευθραυστότητα και αυξημένο κίνδυνο κατάγματος.
Γράφει η
Φούλα Βασιλαρά
Παθολόγος ΥΓΕΙΑ
Η οστεοπόρωση είναι μια συχνή νόσος, η οποία χαρακτηρίζεται από χαμηλή οστική μάζα, διαταραχή της μικροαρχιτεκτονικής του οστού, σκελετική ευθραυστότητα και αυξημένο κίνδυνο κατάγματος. Στο παρόν κείμενο αναλύεται ποιοι ασθενείς θα πρέπει να υποβάλλονται σε έλεγχο για οστεοπόρωση και πώς θα πρέπει να θεραπεύονται.
Πότε πρέπει να υποβάλλονται οι ασθενείς σε μέτρηση οστικής πυκνότητας (άντρες και γυναίκες).
1. Ηλικία • Κατάγματα χαμηλής ενέργειας.
• Υπογοναδισμός.
• Πρώιμη εμμηνόπαυση (• Πρωτοπαθής υπερπαραθυρεοειδισμός.
• Φαρμακευτική αγωγή σχετιζόμενη με απώλεια οστικής μάζας ή και κίνδυνο κατάγματος (π.χ. στεροειδή, αναστολείς αρωματάσης κ.λπ.).
• Έτερα παθολογικά νοσήματα σχετιζόμενα με απώλεια οστικής μάζας ή και κίνδυνο κατάγματος (π.χ. ρευματοειδής αρθρίτιδα, σύνδρομο Cushing, σακχαρώδης διαβήτης τύπου 1, σοβαρή ΧΑΠ κ.λπ.).
2. Ηλικία 50-64 ετών:
• Κάταγμα χαμηλής ενέργειας μετά την ηλικία των 40.
• Κάταγμα ισχίου ή γόνατος.
• Σπονδυλικό κάταγμα ή και οστεοπενική απεικόνιση οστών σε ακτινογραφίες.
• Χαμηλό βάρος (10% από το βάρος του ασθενούς στην ηλικία των 25 ετών.
• Κατανάλωση αλκοόλ (?25-30 γρ./ημερησίως) ή και κάπνισμα.
• Άλλοι παράγοντες και νόσοι (όπως στην ηλικία, ομάδα 3. Ηλικία ?65ετών:
• Όλοι οι άντρες και οι γυναίκες.
Αξιολόγηση μέτρησης οστικής πυκνότητας
• Σε μετεμμηνοπαυσιακές γυναίκες, γυναίκες σε κλιμακτηριακή περίοδο και άντρες ?50 ετών:
o Φυσιολογική οστική πυκνότητα: T-score ±1.0.
o Οστεοπενία: T-score μεταξύ -1.0 και – 2.5
o Οστεοπόρωση: T-score < -2.5.
o Εγκατεστημένη οστεοπόρωση T-score ? -2.5 και ένα ή περισσότερα οστεοπορωτικά κατάγματα.
• Σε γυναίκες και άντρες • Προτιμητέα η χρήση των Z-scores και όχι των T-scores, ενώ οι δόκιμοι όροι για τις ηλικίες αυτές είναι: Οστική πυκνότητα κατώτερη της αναμενόμενης ηλικιακής διακύμανσης Z-score > -2.0.
• Συνιστώμενος εργαστηριακός έλεγχος προ της θεραπείας: Η λήψη του ιστορικού του ασθενούς και η κλινική εξέταση είναι αναντικατάστατες διαδικασίες στην αξιολόγηση του περιστατικού και στον αποκλεισμό δευτεροπαθών αιτίων οστεοπόρωσης.
Ο ελάχιστος απαραίτητος εργαστηριακός έλεγχος προς της έναρξης της θεραπευτικής αγωγής περιλαμβάνει:
• Ασβέστιο ορού (διορθωμένο ως προς την αλβουμίνη ορού).
• Φώσφορο ορού.
• Γενική αίματος.
• ΤΚΕ.
• Κρεατινίνη ορού.
• Αλκαλική φωσφατάση.
• TSH.
• 25(ΟΗ) D3 ορού.
Συνιστώμενος εργαστηριακός έλεγχος προ της θεραπείας: ανάλογα με τα ευρήματα από το ιστορικό, τη φυσική εξέταση και τα αρχικά εργαστηριακά αποτελέσματα είναι δυνατό να απαιτηθεί περαιτέρω εργαστηριακός έλεγχος στα πλαίσια δευτεροπαθών αιτίων οστεοπόρωσης όπως:
• Παραθορμόνη ορού (PTH).
• Τεστοστερόνη ορού (άντρες).
• Ανοσοκαθήλωση ορού και ούρων.
• Κορτιζόλη ούρων 24ώρου.
• Τρυπτάση ορού.
• Αντισώματα έναντι transglutaminase (tTG).
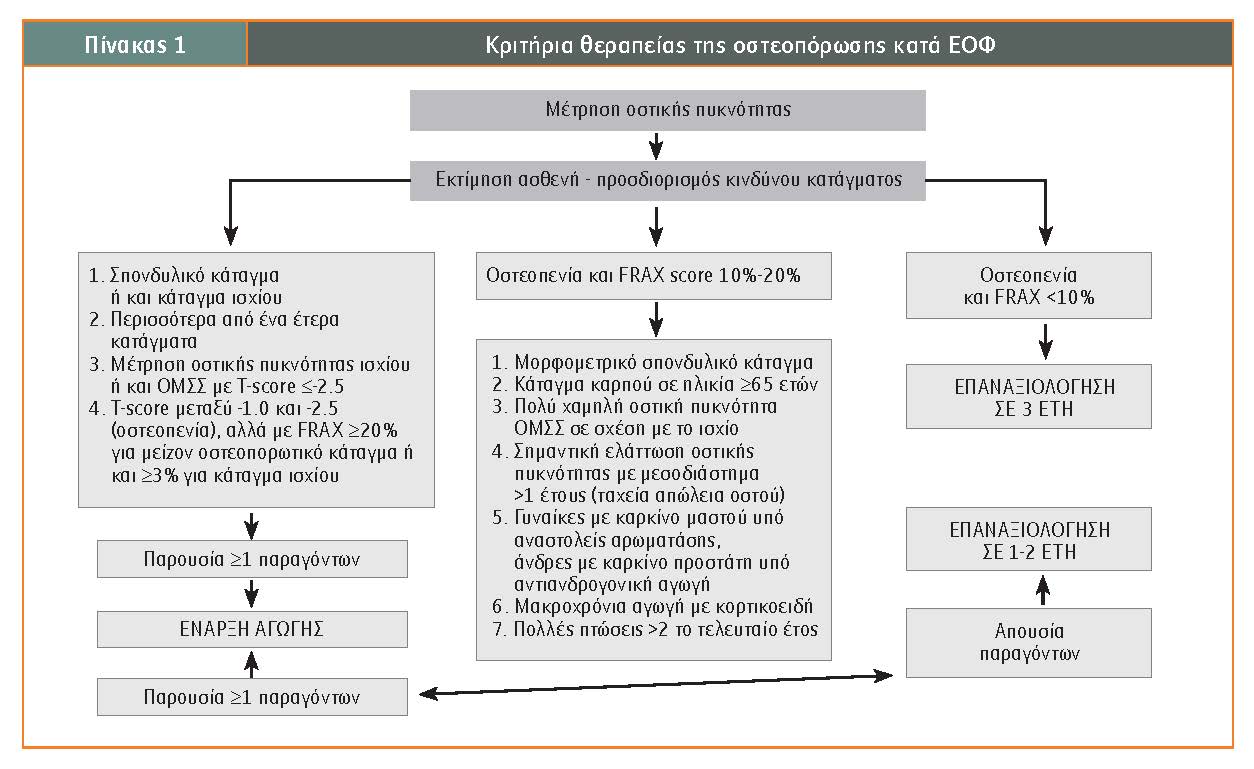
Όπως προκύπτει από τον Πίνακα 1, τα βασικά συμπεράσματα είναι τα ακόλουθα:
1. Όλοι οι ασθενείς με αποδεδειγμένο ακτινολογικό κάταγμα χαμηλής ενέργειας είτε στη σπονδυλική στήλη είτε στο ισχίο θα πρέπει να λαμβάνουν αντιοστεοπορωτική αγωγή ανεξαρτήτως T-score 2).
2. Όλοι οι ασθενείς με T-score ?-2.5 στην ΟΜΣΣ ή στο ισχίο θα πρέπει να λαμβάνουν αντιοστεοπορωτική αγωγή ανεξαρτήτως της παρουσίας ή της απουσίας ακτινολογικού κατάγματος.
Στις υπόλοιπες περιπτώσεις υπολογίζεται το FRAX-SCORE, χρησιμοποιώντας τις διαδικτυακές μηχανές αναζήτησης. Υπάρχει και η ελληνική καταχώριση.
Ανάλογα με την πιθανότητα για μείζον οστεοπορωτικό κάταγμα ή και κάταγμα ισχίου καθορίζεται η αντιοστεοπορωτική αγωγή.
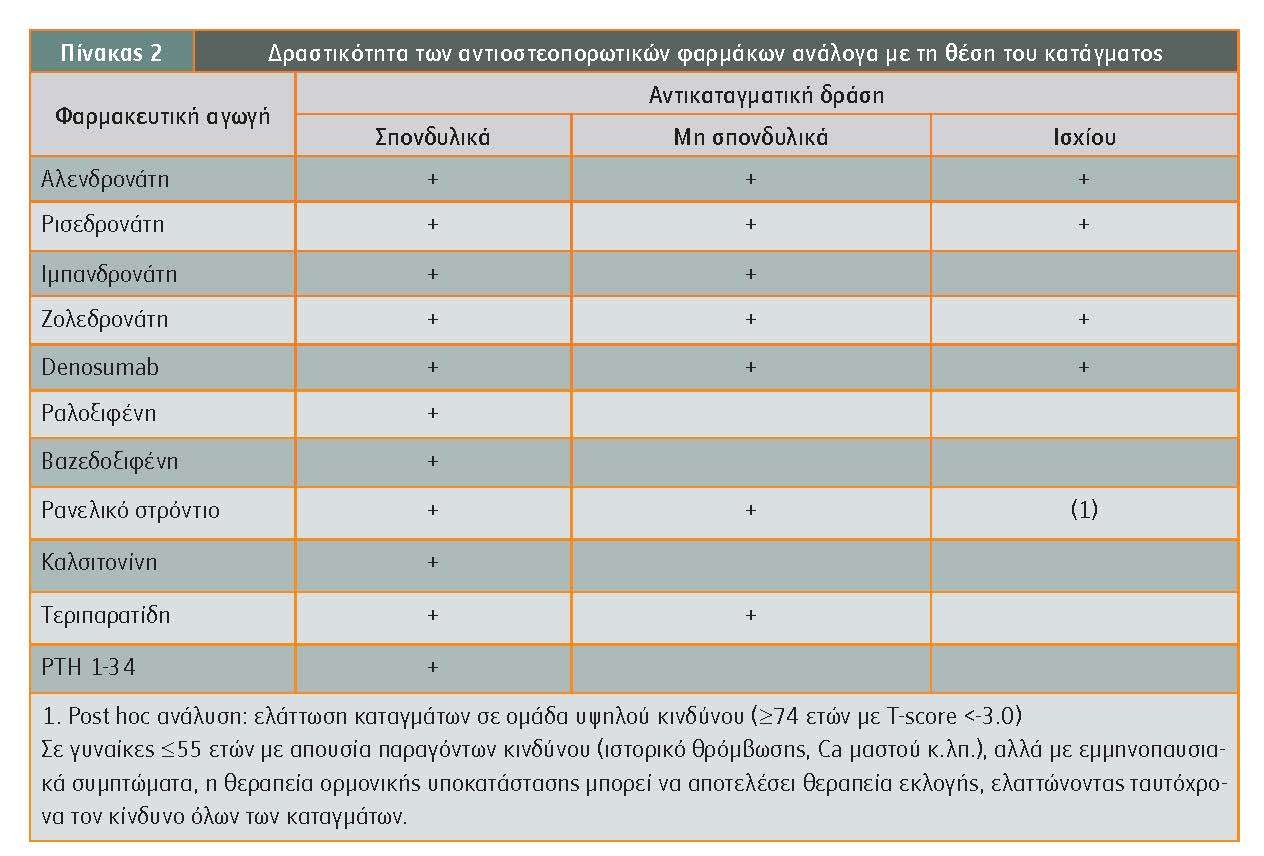
Όλα τα αντιοστεοπορωτικά φάρμακα έχουν αντικαταγματική δράση για τα κατάγματα της ΣΣ. Η ιμπανδρονάτη δεν εξασκεί αντικαταγματική δράση στο ισχίο, όπως επίσης η ραλοξιφένη και η βαζεδοξιφένη δεν εξασκούν αντικαταγματική δράση στα μη σπονδυλικά κατάγματα και στα κατάγματα του ισχίου.
Σύμφωνα με τον Ευρωπαϊκό Οργανισμό Φαρμάκων
(ΕΜΑ) κατά τις τελευταίες οδηγίες του 2014, το ρανελικό στρόντιο θα πρέπει να περιορίζεται σε ασθενείς που δεν έχουν ανταποκριθεί στις υπόλοιπες αντιοστεοπορωτικές αγωγές εξαιτίας του αυξημένου κινδύνου για εν τω βάθει φλεβική θρόμβωση (DVT) και αυξημένο στεφανιαίο κίνδυνο. Επίσης αν αποφασιστεί να χορηγηθεί θα πρέπει να γίνει από εξιδικευμένο γιατρό.
Η καλσιτονίνη επίσης στην οστεοπόρωση περιορίζεται ως αναλγητική αγωγή σε ασθενείς με οστεοπορωτικά κατάγματα και χορηγείται για βραχύ χρονικό διάστημα. Η PTH1- 84 δεν κυκλοφόρησε ποτέ στην Ελλάδα.
Τα διφωσφονικά αποτελούν για πολλές δεκαετίες τη θεραπεία πρώτης επιλογής για την οστεοπόρωση. Τα διφωσφονικά αναστέλλουν τη συνθέτηση του ενζύμου farnesyl diphosphate (FPP) ώστε να μη σχηματίζονται οι farnesylated proteins, οι οποίες είναι απαραίτητες για την επιβίωση και τη δράση των οστεοκλαστών. Έχουν επομένως αντιοστεοκλαστική δράση.
Με την αναστολή των ανωτέρω ενζύμων εκτρέπεται η αντίδραση προς την αυξημένη παραγωγή isopentenyl diphosphate (IPP), ουσία που φαίνεται να σχετίζεται με τη γριπώδη αντίδραση, τα οστικά άλγη και τον πυρετό που παρουσιάζουν οι ασθενείς κυρίως κατά την έγχυση των ενδοφλεβίων διφωσφονικών (π.χ. ζολεντρονικό οξύ).
Πλεονεκτήματα των αμινοδιφωσφονικών:
• Υπάρχει μακρά εμπειρία για την αποτελεσματικότητα και την ασφάλειά τους. Είναι φθηνά και είναι η πρώτη επιλογή θεραπείας.
• Τα αμινοδιφωσφονικά συνδέονται ισχυρά με τον υδροξυαπατίτη και έχουν την ιδιότητα να CεμβυθίζονταιE κάτω από τις οστικές επιφάνειες, όπου παραμένουν για μακρά χρονικά διαστήματα. Έχει υπολογιστεί ότι ο τελικός χρόνος ημισείας ζωής εκτείνεται σε 10 χρόνια. Όταν ο οστεοκλάστης αποδομείται το συνδεδεμένο διφωσφονικό επανακυκλοφορεί τοπικά και συστηματικά και επαναχρησιμοποιείται.
• Στη μελέτη FLEX, η οποία ήταν η συνέχεια της FIT αποδείχθηκε ότι η συνέχιση της αλενδρονάτης σε δόση 5 mg/ημέρα ή 10 mg/ημέρα για 5 επιπλέον χρόνια βελτίωνε περισσότερο την οστική πυκνότητα και μείωνε τα κλινικά σπονδυλικά κατάγματα. Καμία περίπτωση οστεονέκρωσης της γνάθου δεν παρατηρήθηκε, ούτε άτυπα κατάγματα του μηριαίου. Η κύρια παρενέργεια ήταν η αύξηση των γαστρεντερικών διαταραχών σε σχέση με την ομάδα placebo.
Γι? αυτόν ακριβώς το λόγο, όταν υπάρχει δυσανεξία ή αντένδειξη λόγω γαστροοισοφαγικής παλινδρόμησης ή οισοφαγίτιδας στα από του στόματος χορηγούμενα διφωσφονικά, τότε υπάρχει ένδειξη χορήγησης των ενδοφλεβίων διφωσφονικών (zoledronic acid).
Φαίνεται ότι η οστεονέκρωση περιορίζεται στους ογκολογικούς ασθενείς, όπου η αθροιστική δράση είναι μεγάλη και απαιτούνται περαιτέρω μελέτες για να εξαχθούν ασφαλή συμπεράσματα για τον κίνδυνο άτυπων καταγμάτων μηριαίου.
Στην κλινική πράξη για ασθενείς χαμηλού κινδύνου για κατάγματα, η συνήθης πρακτική είναι να διακόπτεται η θεραπεία μετά από 5 χρόνια (drug holiday), ενώ για ασθενείς υψηλού κινδύνου και T-score αυχένα μηριαίου Δεύτερη κατά σειρά συχνότητας αντιοστεοπορωτική αγωγή στην κλινική πράξη αποτελεί η χορήγηση της δενοζουμάμπης (denosumab). Η δενοζουμάμπη αναστέλλει τη σύνδεση του RANKL, ο οποίος εκφράζεται στους οστεοβλάστες με τον υποδοχέα RANK, ο οποίος εκφράζεται από το επίπεδο των προγονικών οστεοκλαστών έως το επίπεδο του ενεργοποιημένου οστεοκλάστη.
Αυτή η αναστολή της σύνδεσης RANK/RANKL επιφέρει αναχαίτιση στη λειτουργία των οστεοκλαστών από τις πρόδρομες έως τις ώριμες μορφές με τελικό αποτέλεσμα την αναστολή της αποδόμησης του οστού. Η οστεοπροτεγερίνη είναι ένας παραπλανητικός υποδοχέας (decoy receptor), η οποία κατά κάποιο τρόπο λειτουργεί όπως και η δενοζουμάμπη, δηλαδή συνδέεται με το RANKL και τον παρεμποδίζει να συνδεθεί με το φυσικό του αναστολέα, δηλαδή το RANK. Με αυτό το μηχανισμό προστατεύεται ο σκελετός από εκτεταμένη οστική απορρόφηση. Άρα η ισορροπία ανάμεσα στο RANKL – RANK – OPG καθορίζει το βαθμό της οστικής απορρόφησης.
Οι ιδιότητες – ενδείξεις και αντενδείξεις της δενοζουμάμπης θα μπορούσαν να συνοψισθούν ως ακολούθως:
• Είναι πλήρως ανθρώπινο μονοκλωνικό αντίσωμα. Αναστέλλει τη σύνδεση RANKL/RANK σε όλες τις πρόδρομες μορφές των οστεοκλαστών μέχρι και τον ώριμο οστεοκλάστη. Αποβάλλεται από το ΔΕΣ και όχι από τους νεφρούς.
• Στη μελέτη FREEDOM και στην επέκτασή της για 3 χρόνια αποδείχθηκε συνεχόμενη αύξηση της BMD στην ΟΜΣΣ έως 15% και 7,5% στο ολικό ισχίο και μείωση του ποσοστού των καταγμάτων ανεξαρτήτως θέσης.
• Παρενέργειες: παρατηρήθηκαν 4 περιπτώσεις οστεονέκρωσης της γνάθου, μία περίπτωση άτυπου κατάγματος του μηριαίου, συμπτωματική υπασβεστιαιμία, ενδεχομένως αυξημένος κίνδυνος λοιμώξεων και κακοηθειών.
Η δενοζουμάμπη δε διαθέτει ευθέως συγκριτικές μελέτες με άλλες αντιοστεοπορωτικές αγωγές. Έτσι θα πρέπει να θεωρείται θεραπεία πρώτης επιλογής σε ασθενείς με σοβαρή νεφρική ανεπάρκεια και GFR Η τεριπαρατίδη ή ανασυνδυασμένη παραθορμόνη αποτελεί τη μόνη εγκεκριμένη αναβολική θεραπεία για την οστεοπόρωση. Δρα στο μονοπάτι Wnt και διεγείρει τους οστεοβλάστες με αποτέλεσμα τη δημιουργία νέου οστού.
Οι ενδείξεις χορήγησης τεριπαρατίδης 20 mg/ημέρα υποδορίως για 18-24 μήνες είναι οι ακόλουθες:
• Ασθενείς με αντένδειξη σε διφωσφονικά ή αποτυχία σε άλλες θεραπείες.
• Μετεμηνοπαυσιακές γυναίκες/άντρες: αγωγή 1ης επιλογής σε γυναίκες με 2 ή περισσότερα σπονδυλικά κατάγματα και T-score ?-2.5 SD ή σε γυναίκες με 1 σπονδυλικό κάταγμα και T- score ?-3.5SD.
• Οστεοπόρωση από κορτικοειδή: αγωγή 1ης επιλογής σε ασθενείς με οστεοπόρωση και σπονδυλικό κάταγμα ή T – score ?-2.5 SD και αντένδειξη για διφωσφονικά.
• Είναι κοινή πρακτική να ακολουθείται μετά τη χορήγηση της τεριπαρατίδης θεραπεία με διφωσφονικά λόγω της ταχείας απώλειας του οστού μετά τη διακοπή της πρώτης.
• Η δράση της τεριπαρατίδης μειώνεται σε ασθενείς που προηγήθηκε θεραπεία με διφωσφονικά. Οι κύριες ανεπιθύμητες παρενέργειές της είναι η υπερασβεστιαιμία, η υπερασβεστιουρία, η υπερουριχαιμία. Σε ασθενείς με ιστορικό οστεοσαρκώματος αποτελεί αντένδειξη η χορήγησή της.
Σε όλες τις περιπτώσεις θεραπείας της οστεοπόρωσης (άντρες και γυναίκες) κρίνεται σκόπιμη η συγχορήγηση 400-800 IU βιταμίνης D3, αλλά και η πρόσληψη (διαιτητική ή και φαρμακευτική) 1.200 mg ασβεστίου/ημέρα.
Η συνεχής σύσταση για σωματική άσκηση, αποφυγή του καπνίσματος και κατάχρηση αλκοόλ, καθώς και η προφύλαξη από τον κίνδυνο πτώσεων θα πρέπει να ενθαρρύνεται με συστηματικό τρόπο.
Ειδικές περιπτώσεις – επισημάνσεις:
• Σε ασθενείς με πρόσφατο σπονδυλικό κάταγμα δύναται να συγχορηγηθεί καλσιτονίνη λόγω της αναλγητικής της δράσης. Αναλγητική δράση στον οσφυϊκό πόνο έχει αναφερθεί και με την τεριπαρατίδη.
• Σε ασθενείς με σοβαρή νεφρική ανεπάρκεια θεραπεία πρώτης επιλογής αποτελεί το denosumab.
• Σε γυναίκες που έχει χορηγηθεί αγωγή με τεριπαρατίδη, πρέπει να ακολουθήσει αντι-οστεοκλαστική αγωγή (π.χ. διφωσφονικά).
• Σε γυναίκες με αυξημένο κίνδυνο εμφάνισης καρκίνου μαστού μπορεί να προτιμηθεί αρχικά η ραλοξιφένη.
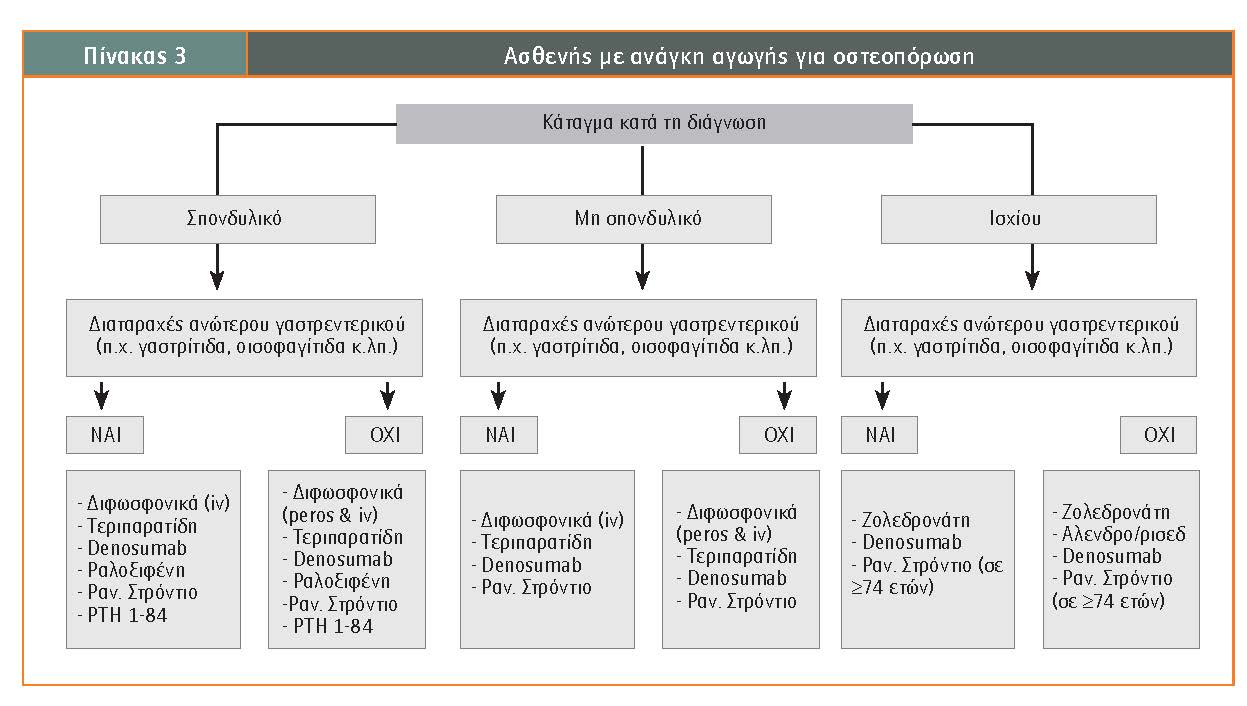
Όλα τα ανωτέρω μπορούν να σχηματοποιηθούν σύμφωνα με τις οδηγίες του ΕΟΦ στον Πίνακα 3.
Αναδυόμενες θεραπείες:
• Odanacatib: Αποτελεί νέο αντι-οστεοκλαστικό παράγοντα και βρίσκεται σε κλινικές μελέτες φάσης ΙΙΙ σε γυναίκες με μετεμηνοπαυσιακή οστεοπόρωση. Αναστέλλει τη καθεψίνη Κ, η οποία είναι ένζυμο του λυσοσώματος των οστεοκλαστών και έτσι μειώνει την οστική απορρόφηση.
• Romosozumab: Είναι μονοκλωνικό αντίσωμα. Δρα έναντι της πρωτεΐνης sclerostin, η οποία εκκρίνεται από τα οστεοκύτταρα. Τα οστεοκύτταρα φαίνεται να αποτελούν τον CμηχανοστάτηE του οστικού μεταβολισμού. Έχουν την ιδιότητα να αναγνωρίζουν τα μικροκατάγματα/μικρορωγμές και υπάρχει έντονο σύγχρονο ενδιαφέρον για το ρόλο των οστεοκυττάρων στον οστικό μεταβολισμό. Η sclerostin είναι η πρωτεΐνη που μειώνει τον οστικό μεταβολισμό αναστέλλοντας το Wnt μονοπάτι στο επίπεδο του οστεοβλάστη. Με την αναστολή/εξουδετέρωση αυτής της πρωτεΐνης (sclerostin) αφήνεται ελεύθερο το Wnt μονοπάτι και αυξάνεται επομένως ο σχηματισμός νέου οστού.
Bιβλιογραφία
Κατευθυντήριες Γραμμές για τη διάγνωση και αντιμετώπιση της οστεοπόρωσης στην Ελλάδα. Ελληνικό Ίδρυμα Οστεοπόρωσης 2013.
European Guidance for the diagnosis and management of osteoporosis in postmenopausal women ESCEO / IOF. Osteoporos Int 2012.
Bone HG, Chapurlat R, Brandi ML, et al. The effect of three or six years of denosumab exposure in women with postmenopausal osteoporosis: results from the FREEDOM extension. J Clin Endocrinol Metab. 2013; 98(11): 4.483.
Black DM, Schwartz AV, Ensrud KE, et al. Effects of continuing or stopping alendronate after 5 years of treatment: the Fracture Intervention Trial Long-term Extension (FLEX): a randomized trial. JAMA, 2006; 296(24): 2.927-2.938.
Bone HG, Hosking D, Devogelaer JP, et al. Ten years’ experience with alendronate for osteoporosis in postmenopausal women. N Engl J Med 2004; 350: 1.189-1.199.
Abrahamsen B, Eiken P, Eastell R. Subtrochanteric and diaphyseal femur fractures in patients treated with alendronate: a register-based national cohort study. Bone Miner Res 2009; 24: 1.095-1.102.
Rizzoli R, Kraenzlin M, Krieg MA, et al. Indications to teriparatide treatment in patients with osteoporosis. Swiss Med Wkly, 2011; 141: w13297.
Nanional Osteoporosis Fοundation, 2014.
Kramer I, Keller H, Leupin O, et al. Does osteocytic SOST suppression mediate PTH bone anabolism? Trends Endocrinol Metab 2010; 21(4): 237-244.
Khan A, Fortier M, for the menopause osteoporosis working group. J Obstet Gynaecol Can 2014; 36(9eSuppl C): S1-S15.
Φεβρουάριος 2016