Διαγνωστικός χειρισμός γυναικών με υποψία καρκίνου του μαστού – Μαγνητική μαστογραφία (MRM)
H μαγνητική μαστογραφία είναι μέθοδος ευρέως αποδεκτή στις περισσότερες ανεπτυγμένες χώρες.
Γράφει η
Βασιλική Φιλιππή
Ακτινολόγος
Επιμελήτρια Τμήματος Αξονικής και Μαγνητικής Τομογραφίας ΥΓΕΙΑ, ΜΗΤΕΡΑ
Στην Ελλάδα δεν έχει ενσωματωθεί στην καθημερινή κλινική πράξη και εφαρμόζεται σε λίγα κέντρα. Οι λόγοι είναι κυρίως δύο: η ανεπαρκής ενημέρωση των κλινικών ιατρών που ασχολούνται με τα προβλήματα του μαστού, σχετικά με τις ενδείξεις και τους περιορισμούς της μεθόδου, καθώς και οι τεχνικές ιδιαιτερότητες της εξέτασης.
H ακρίβεια της εξέτασης εξαρτάται από τον εξοπλισμό, την επιλογή ασθενών και χρόνου εξέτασης, την εφαρμοζόμενη τεχνική, την εφαρμογή συγκεκριμένων διαγνωστικών κριτηρίων και την πείρα του διαγνώστη.
Η μαγνητική μαστογραφία προγραμματίζεται αφού αξιολογηθούν το ιστορικό και τα ευρήματα της κλινικής εξέτασης της ασθενούς, καθώς και τα ευρήματα μιας πρόσφατης, καλής ποιότητας μαστογραφίας ή και υπερηχογραφήματος, για να εκτιμηθεί αν υπάρχει ένδειξη.
Γυναίκες αναπαραγωγικής ηλικίας είναι προτιμότερο να υποβάλλονται σε μαγνητική μαστογραφία μεταξύ 7ης και 14ης ημέρας του εμμηνορρυσιακού κύκλου, για να μειωθεί η πιθανότητα ψευδώς θετικών ευρημάτων. Για τον ίδιο λόγο γυναίκες σε εμμηνόπαυση που λαμβάνουν θεραπεία ορμονικής υποκατάστασης, είναι καλύτερα να τη διακόπτουν για 6-8 εβδομάδες πριν από την εξέταση.
Όπως σε κάθε περίπτωση που προγραμματίζεται μια εξέταση στο μαγνητικό τομογράφο, θα πρέπει να αποκλείεται η ύπαρξη πιθανών αντενδείξεων, όπως η παρουσία καρδιακού βηματοδότη και μεταλλικών ξένων σωμάτων σε ζωτικά σημεία του σώματος. Επίσης, θα πρέπει να διερευνάται η περίπτωση της κλειστοφοβίας, καθώς για την επιτυχία μιας εξέτασης μαγνητικής μαστογραφίας απαιτείται πλήρης συνεργασία, ηρεμία και ακινησία της εξεταζόμενης. Αν κριθεί απαραίτητο, μπορεί να δοθεί ήπια νάρκωση.
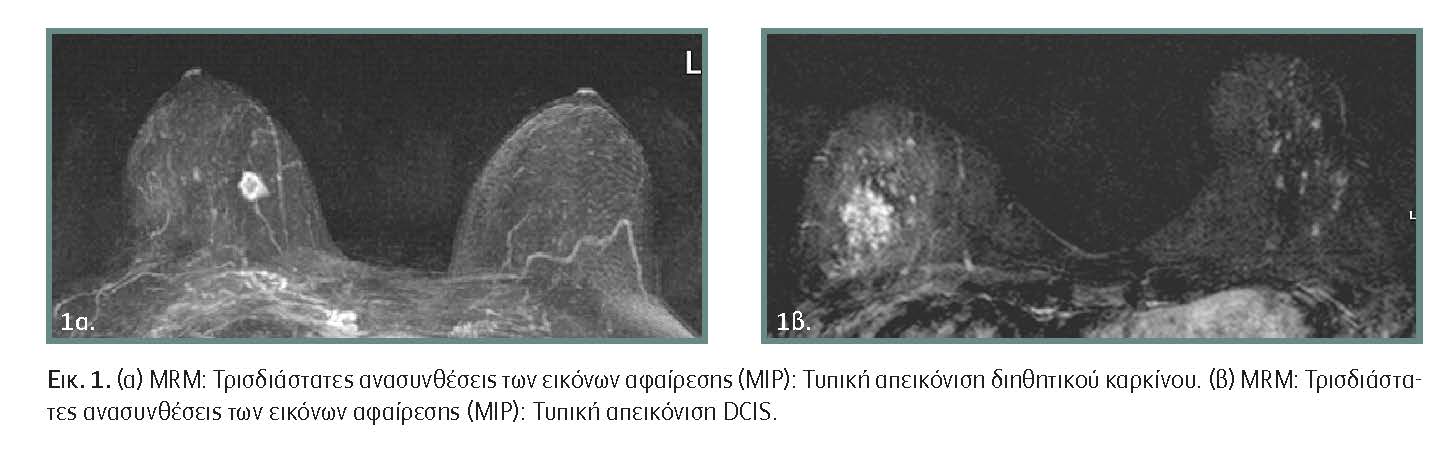
Συγκριτικά με τις υπόλοιπες τεχνικές απεικόνισης του μαστού (μαστογραφία και υπερηχογράφημα) η μαγνητική μαστογραφία έχει μεγαλύτερη ευαισθησία στο διηθητικό καρκίνο του μαστού.
Τα ποσοστά ευαισθησίας στη βιβλιογραφία κυμαίνονται από 89% έως 100% και είναι μεγαλύτερα από αυτά της μαστογραφίας. Ο βαθμός στον οποίο η ευαισθησία της μαστογραφίας και μαγνητικής μαστογραφίας διαφέρουν στον ίδιο ασθενή εξαρτάται από την πυκνότητα των μαστών και τον τύπο του καρκίνου. Η ευαισθησία της μαγνητικής μαστογραφίας δεν επηρεάζεται από την πυκνότητα του αδένα και από ουλώδη ιστό έπειτα από εγχείρηση, ακτινοβολία ή την παρουσία ενθεμάτων.
Η ευαισθησία στον πορογενή in situ καρκίνο του μαστού είναι χαμηλότερη συγκριτικά με τον διηθητικό καρκίνο, λόγω ήπιας αγγειογενετικής δραστηριότητας, η οποία συνήθως απεικονίζεται με «καλόηθες» πρότυπο πρόσληψης του σκιαγραφικού. Με την εφαρμογή συγκεκριμένων διαγνωστικών κριτηρίων, η μαγνητική μαστογραφία μπορεί να αναδείξει 40% των DCIS (κυρίως των high-grade), τα οποία δεν αναδεικνύονται με τη μαστογραφία.
Στη συνέχεια, αναφέρονται τα οφέλη αλλά και τα προβλήματα που προκύπτουν από την εφαρμογή της μαγνητικής μαστογραφίας στις κύριες κλινικές της ενδείξεις.
Αμφίβολα ευρήματα στο συμβατικό απεικονιστικό έλεγχο
Η ευαισθησία της μαγνητικής μαστογραφίας στην ανάδειξη του καρκίνου είναι μεγαλύτερη από εκείνη των άλλων τεχνικών. Γενικά, η αρνητική μαγνητική μαστογραφία σχεδόν αποκλείει το διηθητικό καρκίνο. Μόνο στην περίπτωση της ύπαρξης μικροαποτιτανώσεων δεν είναι δυνατό να αποκλειστεί η ύπαρξη καρκίνου και η απόφαση για βιοψία πρέπει να βασίζεται στα ευρήματα της μαστογραφίας.
Συνήθεις περιπτώσεις όπου η συμβολή της μαγνητικής μαστογραφίας είναι σημαντική για τη λήψη αποφάσεων, αποτελούν εκείνες κατά τις οποίες τίθεται ζήτημα:
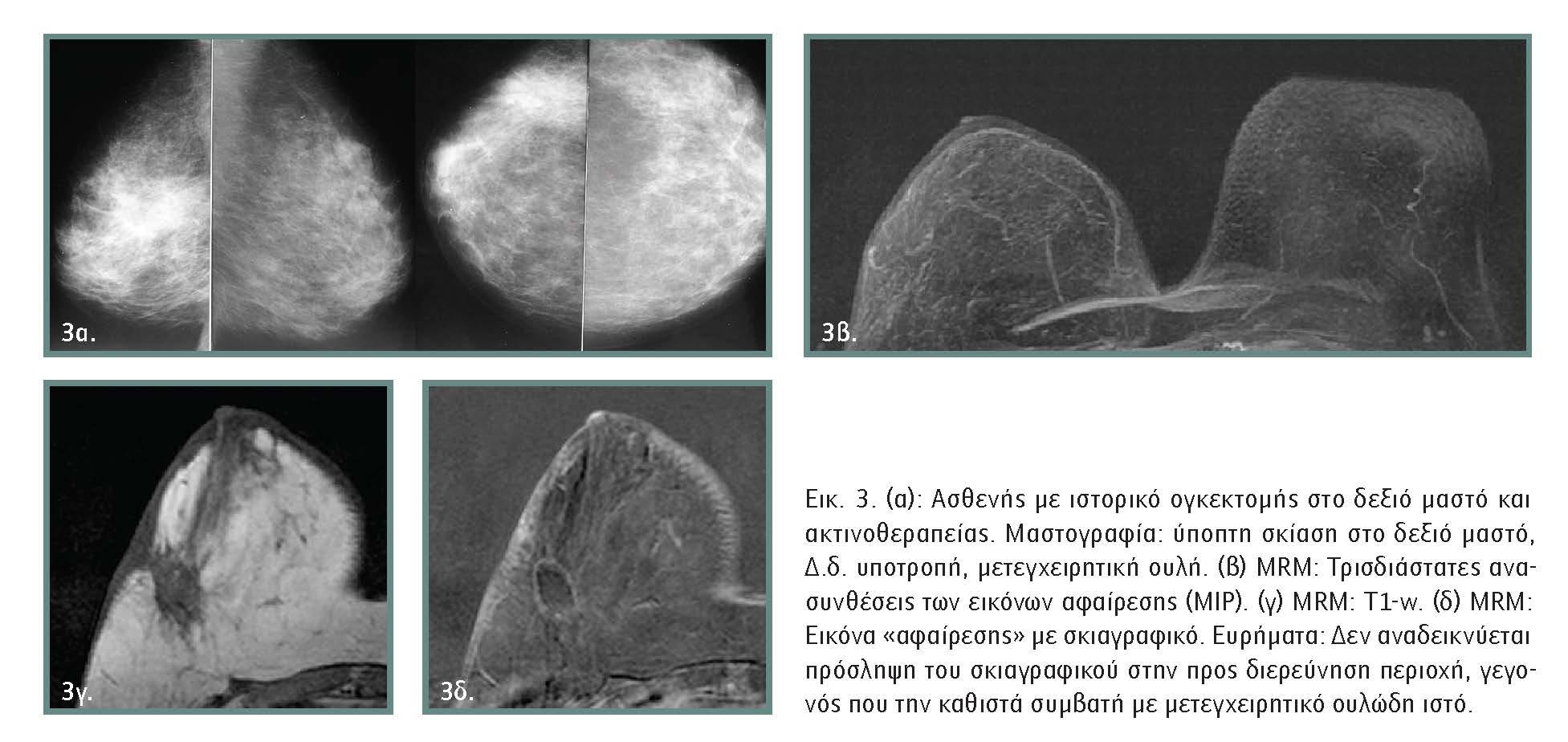
- διαφορικής διάγνωσης μεταξύ μεταθεραπευτικής ουλής και υποτροπής καρκίνου,
- διάκρισης άτυπης καλοήθους βλάβης (όπως κύστης είτε με παχύρρευστο περιεχόμενο είτε επιπλακείσας, ινοαδενώματος) από καρκίνο,
- αξιολόγησης εστιακής ή περιοχικής ασυμμετρίας, χωρίς αποτιτανώσεις, στη μαστογραφία,
- διερεύνησης ευρήματος που είναι εμφανές μόνο σε μια προβολή της μαστογραφίας,
- αξιολόγησης ύποπτων μικροαποτιτανώσεων στη μαστογραφία.
Στις περιπτώσεις 1 και 4 και χάρη στην υψηλή της αρνητική προγνωστική αξία (NPV), αν με τη μαγνητική μαστογραφία εκτιμηθεί ότι πρόκειται για καλοήθη βλάβη, περιορίζεται η ανάγκη βιοψίας. Στην περίπτωση 5 πρέπει να τονιστεί ότι η απόφαση για βιοψία ύποπτων μικροαποτιτανώσεων θα πρέπει να στηρίζεται αποκλειστικά στην εντύπωση που δίνουν στη μαστογραφία και ότι, για τη διάγνωση του DCIS και την εκτίμηση της έκτασής του, ο ρόλος των δύο εξετάσεων είναι συμπληρωματικός.
Από ορισμένους συγγραφείς προτείνεται να μη χρησιμοποιείται συμπληρωματικά η μαγνητική μαστογραφία για το χαρακτηρισμό αμφίβολων ευρημάτων στο συμβατικό απεικονιστικό έλεγχο όταν οι βλάβες μπορούν να διερευνηθούν με βιοψία.
Προεγχειρητικός έλεγχος
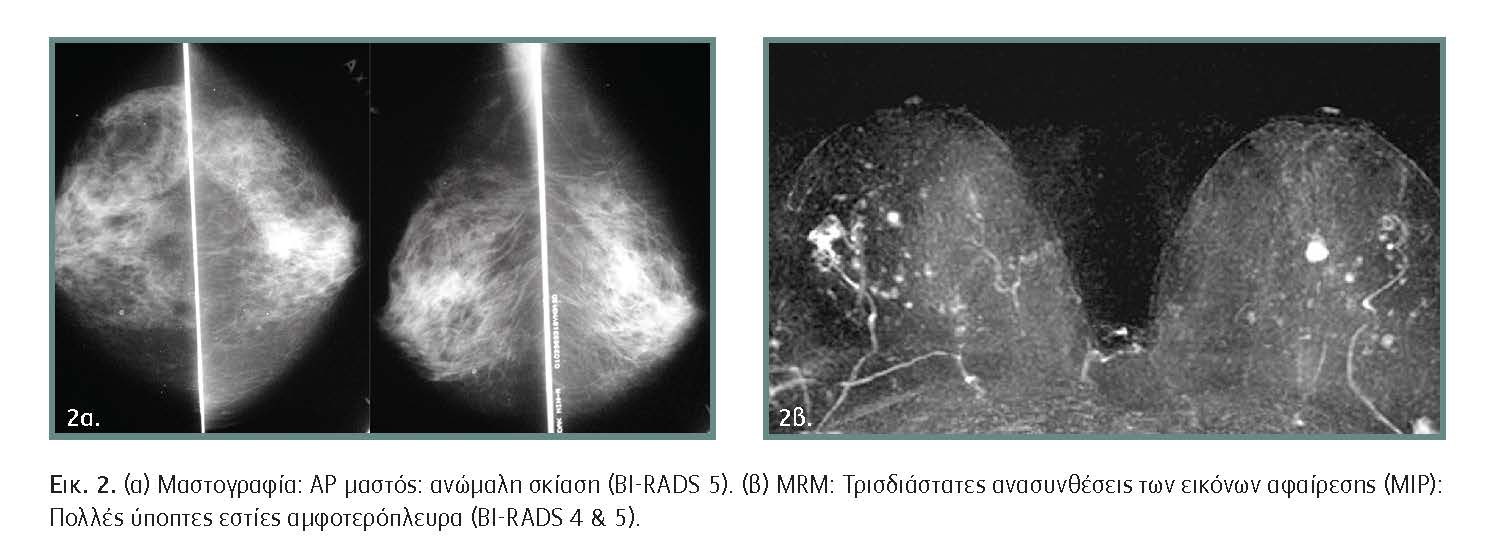
Το μέγεθος των όγκων του καρκίνου του μαστού είναι δυνατό να υποεκτιμάται στη μαστογραφία και στο υπερηχογράφημα, ειδικά σε όγκους διαμέτρου μεγαλύτερης των 2 εκ. Αντιθέτως, το μέγεθος των διηθητικών καρκίνων στη μαγνητική μαστογραφία ανταποκρίνεται με ακρίβεια στο πραγματικό μέγεθος του όγκου, αν και υπάρχει η τάση να υπερεκτιμάει το μέγεθος των DCIS. Ανεπαρκής εκτίμηση του μεγέθους του όγκου μπορεί να έχει ως αποτέλεσμα διηθημένα εγχειρητικά όρια. Επιπλέον σε ποσοστό 25% των περιπτώσεων καρκίνου του μαστού ο όγκος είναι πολυεστιακός και σε ποσοστό 20% πολυκεντρικός.
Η ευαισθησία της μεθόδου στην προεγχειρητική σταδιοποίηση είναι 100%. Είναι η πιο αξιόπιστη μέθοδος για τον υπολογισμό του μεγέθους του όγκου και αναδεικνύει επιπλέον εστίες στο 10%-30% των ασθενών. Επιπλέον αξιολογεί καλύτερα τυχόν ενδοπορικό τμήμα του όγκου, αν και σε ποσοστό 20% οι επιπρόσθετες εστίες που αναδεικνύονται είναι καλοήθεις.
Αρκετές μελέτες δείχνουν αλλαγή στη διαχείριση σε ποσοστό 20%-30%. Οι αλλαγές είναι συχνότερες σε όγκους μεγαλύτερους των 4 εκ., σε λοβιακό καρκίνο και σε πυκνούς μαστούς.
Σύγχρονος αμφοτερόπλευρος καρκίνος αναφέρεται σε ποσοστά 2%-3%, αν και είναι πιθανό να είναι συχνότερος. Οι σύγχρονοι καρκίνοι συχνά δεν αναδεικνύονται σε ποσοστό μέχρι 75%. Η μαγνητική μαστογραφία εντοπίζει αυτούς τους όγκους σε ποσοστό 5%-24%, οι οποίοι θα κατηγοριοποιούνταν διαφορετικά ως μετάχρονοι καρκίνοι. Με τη συμπληρωματική μελέτη με μαγνητική τα ποσοστά ετερόπλευρων καρκίνων κατά την μετεγχειρητική παρακολούθηση μειώθηκαν από το 4% στο 1,7%.
Η προεγχειρητική σταδιοποίηση με μαγνητική μαστογραφία είναι ιδιαίτερα χρήσιμη σε ασθενείς με πυκνούς μαστούς και σε ασθενείς με ιστολογική επιβεβαίωση διηθητικού λοβιακού καρκίνου, καθώς αυτή η κατηγορία όγκων χαρακτηρίζεται από διάχυτα διηθητικό (permeative) πρότυπο ανάπτυξης, το οποίο καθιστά δύσκολη τη μέτρηση των διαστάσεων του όγκου και είναι συχνότερα πολυκεντρικό και πολυεστιακό (32%).
Προσυμπτωματικός έλεγχος γυναικών υψηλού κινδύνου για καρκίνο μαστού
Οι γυναίκες σε υψηλό κίνδυνο για ανάπτυξη καρκίνου μαστού, αποτελούν έναν ετερογενή πληθυσμό, στον οποίο υπάγονται ομάδες:
- φορέων γονιδιακών μεταλλάξεων (BRCA1, BRCA2, PTEN, TP53, CHECK, κ.ά.),
- γυναικών με ατομικό ή ισχυρό οικογενειακό ιστορικό καρκίνου είτε του μαστού είτε των ωοθηκών,
- με ιστορικό βιοψίας μαστού που ανέδειξε προκαρκινική βλάβη ή ατυπία (όπως ακτινωτή ουλή, άτυπη επιθηλιακή υπερπλασία-ADH, λοβιακό καρκίνο in situ-LCIS), και
- γυναίκες με ιστορικό ακτινοθεραπείας του θώρακα σε νεαρή ηλικία (όπως σε περιπτώσεις λεμφώματος).
Η προσυμπτωματική διάγνωση του οικογενούς και κληρονομικού καρκίνου του μαστού είναι δύσκολη. Η μαστογραφία μπορεί να διαγνώσει λιγότερους από τους μισούς καρκίνους που εμφανίζονται στις φορείς γονιδιακών μεταλλάξεων BRCA, κυρίως λόγω του πυκνού μαστού αυτών των νεαρών γυναικών και του γρήγορου ρυθμού ανάπτυξης των όγκων.
Πραγματικά, σε αυτές τις γυναίκες το 43%-60% των καρκίνων γίνονται αντιληπτοί κλινικά μεταξύ των ετήσιων προσυμπτωματικών ελέγχων, έχουν μέση διάμετρο 1,7 εκ. και τουλάχιστον οι μισοί από αυτούς έχουν ήδη δώσει λεμφαδενικές μεταστάσεις τη στιγμή της διάγνωσης.
Τα τελευταία χρόνια δημοσιεύθηκαν τα αποτελέσματα αρκετών μελετών που αξιολόγησαν τις διαγνωστικές επιδόσεις της μαγνητικής μαστογραφίας σε σύγκριση με τον συμβατικό έλεγχο σε γυναίκες υψηλού κινδύνου. Όλες συγκλίνουν στο ότι η πρώιμη διάγνωση του καρκίνου του μαστού βελτιώνεται σημαντικά όταν η μαγνητική μαστογραφία περιλαμβάνεται στο ετήσιο πρόγραμμα προσυμπωματικού ελέγχου.
Στις μελέτες αυτές, η ευαισθησία της μαγνητικής μαστογραφίας κυμάνθηκε στο 79%-98%. Η θετική προγνωστική αξία (PPV) της μεθόδου (35%-64%) δεν είναι ιδεώδης, αλλά θεωρείται αποδεκτή, συγκρινόμενη με τη χαμηλότερη αντίστοιχη επίδοση της μαστογραφίας και του υπερηχογραφήματος.
Μειονέκτημα της μεθόδου αποτελεί η αυξημένη συχνότητα ψευδών θετικών διαγνώσεων, η οποία ωστόσο μειώνεται προοδευτικά στους επόμενους επανελέγχους, ώστε στη μελέτη του Warner και συν. να φθάνει στο επίπεδο της μαστογραφίας κατά τον 4ο ετήσιο κύκλο. Η παρατήρηση αυτή δείχνει ότι η μειωμένη ειδικότητα και PPV δεν είναι εγγενές πρόβλημα της εξέτασης, αλλά κυρίως ζήτημα απόκτησης πείρας από τη χρήση της.
Σύμφωνα με πρόσφατη οδηγία της Αμερικανικής Αντικαρκινικής Εταιρείας, συνιστάται ετήσιος προσυμπτωματικός έλεγχος με μαγνητική μαστογραφία όλων των γυναικών που:
- Είναι αποδειγμένα φορείς μετάλλαξης BRCA1, BRCA2, TP53 ή PTEN είτε έχουν πρώτου βαθμού συγγένεια με φορέα τέτοιας γονιδιακής μετάλλαξης.
- Έχουν διά βίου πιθανότητα ανάπτυξης καρκίνου μαστού μεγαλύτερη ή ίση του 20%, σύμφωνα με μοντέλα υπολογισμού κινδύνου που στηρίζονται στην παρουσία ισχυρού οικογενειακού ιστορικού καρκίνου μαστού ή ωοθηκών.
- Υποβλήθηκαν σε ακτινοθεραπεία θώρακα σε ηλικία 10-30 ετών για νόσο Hodgkin.
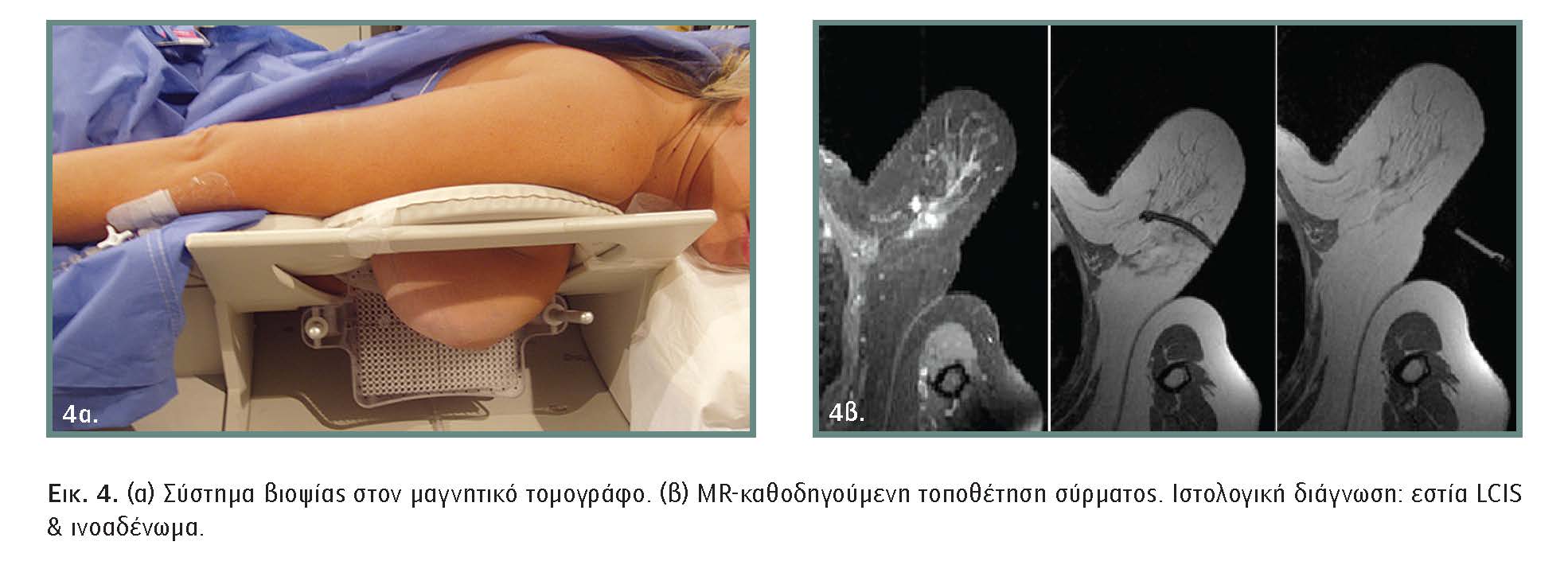
Για τη μεγιστοποίηση του οφέλους από την υψηλή ευαισθησία της μεθόδου, καθώς υπάρχουν βλάβες που αναδεικνύονται μόνο με μαγνητική μαστογραφία, είναι ουσιώδες να υπάρχει η δυνατότητα MR καθοδηγούμενης βιοψίας.
Έχουν αναπτυχθεί τεχνικές για διαδερμική βιοψία (λήψη ιστοτεμαχιδίων ή βιοψία CκενούE-vacuum biopsy) ή σήμανση αυτών με MR-καθοδήγηση. Βιοψία είναι, γενικά, εφικτή σε βλάβες διαμέτρου μεγαλύτερης του 1 εκ., ενώ για εστίες μικρότερες του 1 εκ. προτείνεται σήμανση με ειδικό σύρμα και χειρουργική εξαίρεση. Επίσης, έχουν περιγραφεί τεχνικές MR καθοδηγούμενης διαδερμικής κατάλυσης (thermal ablation) μικρών όγκων του μαστού.
Μεταστατικός καρκίνος αγνώστου πρωτοπαθούς αιτιολογίας
Σε κλινική υποψία καρκίνου του μαστού και αρνητικό μαστογραφικό έλεγχο, σύμφωνα με τη βιβλιογραφία στο 50% των περιπτώσεων υπάρχουν ευρήματα στη μαγνητική μαστογραφία. Στην περίπτωση που υπάρχουν διηθημένοι μασχαλιαίοι λεμφαδένες, η μαγνητική μαστογραφία αναδεικνύει τον πρωτοπαθή όγκο στο 75%-85% των ασθενών, επηρεάζοντας την επιλογή κατάλληλης θεραπείας.
Bιβλιογραφία
1. Ρουσάκης Α. Μαγνητική Μαστογραφία, στο Σύγχρονη Μαστολογία. Ιωαννίδου – Μουζάκα Λ, εκδ. Πασχαλίδης, Αθήνα 2007: 347-387.
2. Kuhl CK. The current status of breast MR imaging: part I. Choice of technique, image interpretation, diagnostic accuracy, and transfer to clinical practice. Radiology 2007; 244: 356-378.
3. Kuhl CK. The current status of breast MR imaging: part 2. Clinical Applications. Radiology 2007; 244 (3): 672-691.
4. Sardanelli F, Giuseppetti GM, Canavese G, et al. Indications for breast magnetic resonance imaging. Consensus document Attualita in senologia, 2007. La radiologia medica, 2008; 113: 1.085-1.095.
5. Causer P, Jong R, Warner E, et al. Breast cancers detected with imaging screening in the BRCA population: emphasis on MR imaging with histopathologic correlation. RadioGraphics, 2007; 27: s165-S182.
6. Mann RM, Kuhl CK, Kinkel K, et al. Breast MRI: guidelines from the European Society of Breast Imaging. Eur Radiol. 2008 July; 18: 1.307-1.318.
7. Smith RA. The evolving role of MRI in the detection and evaluation of breast cancer. N Engl J Med 2007; 356: 1.362-1.364.
Οκτώβριος 2016