Η σημασία της FNA για τη διάγνωση και την αντιμετώπιση βλάβης του μαστού
Παρά την εκτεταμένη πρόοδο όσον αφορά στην επιδημιολογία, διάγνωση και αντιμετώπιση του καρκίνου του μαστού, ο συγκεκριμένος καρκίνος εξακολουθεί να είναι από τους πλέον συχνούς στο γυναικείο πληθυσμό.
Γράφουν οι
Γεωργία-Ελένη Θωμοπούλου
Μαρία Κάλφα
Ειρήνη Κλαψινού
Κυτταρολόγοι, Κυτταρολογικό Εργαστήριο ΥΓΕΙΑ-ΜΗΤΕΡΑ
Υπολογίζεται ότι περίπου 180.000 νέες περιπτώσεις καρκίνου του μαστού διαγιγνώσκονται κάθε χρόνο στις ΗΠΑ και περίπου 30.000 στο Ηνωμένο Βασίλειο. Είναι δε η κύρια αιτία θανάτου γυναικών ηλικίας 35-54 ετών.
Η παρακέντηση μαστού με λεπτή βελόνη (FNA) είναι ευρέως αποδεκτή διαγνωστική μέθοδος, που έχει αντικαταστήσει σε πολλές περιπτώσεις την ανοιχτή χειρουργική βιοψία και έχει καταστήσει δυνατό τον καθορισμό της οριστικής θεραπείας προεγχειρητικά.
Η έγκαιρη διάγνωση του καρκίνου του μαστού παίζει σημαντικό ρόλο στην πρόγνωση και την επιβίωση της ασθενούς. Ψηλαφητές αλλοιώσεις μπορούν θαυμάσια να παρακεντηθούν με λεπτή βελόνη (23G ή μικρότερη), ενώ είναι δυνατή η παρακέντηση ακόμη και μικρότερων, μη ψηλαφητών αλλοιώσεων, με τη βοήθεια απεικονιστικών τεχνικών, κυρίως υπερηχοτομογράφου.
Η Cτριπλή διαγνωστική προσέγγισηE, που περιλαμβάνει ψηλάφηση, απεικονιστικά ευρήματα και FNA, εφαρμόζεται σε καλοήθεις, προνεοπλασματικές, οριακής κακοήθειας ή κακοήθεις αλλοιώσεις μαστού. Η εκτέλεση και η ερμηνεία της FNA απαιτούν επαρκή εκπαίδευση και πείρα.
Οι περιπτώσεις που αναφέρονται από τους κυτταρολόγους ως Cκυτταρολογική ατυπίαE (η λεγόμενη γκρίζα ζώνη) υπολογίζονται στη διεθνή βιβλιογραφία από 1% έως 22%, με μέσο όρο 10% στις περισσότερες μελέτες. Μάλιστα, κάθε προσπάθεια θα πρέπει να στραφεί στην ελαχιστοποίηση των CάτυπωνE κυτταρολογικών διαγνώσεων.
Συνολικά, η FNA μαστού είναι εξαιρετικά επιτυχής, με ευαισθησία που κυμαίνεται στο 80%-100% και ειδικότητα >99%. Επιπλέον, σχεδόν σε επίπεδο ρουτίνας, πέρα από την ακριβή διάγνωση που παρέχει, μπορεί να χρησιμοποιηθεί για την ανάλυση της βιολογικής συμπεριφοράς του όγκου εκτιμώντας το επίπεδο οιστρογονικών/προγεστερονικών υποδοχέων, δεικτών κυτταρικού πολλαπλασιασμού, καθώς και για τον καθορισμό προγνωστικών δεικτών όπως την έκφραση Her2neu.
Εδώ αξίζει να αναφέρουμε ότι το κυτταρολογικό εργαστήριο του Ομίλου ΥΓΕΙΑ είναι από τα ελάχιστα στην Ελλάδα που διαθέτουν τον εξοπλισμό, την υποδομή και την εκπαίδευση για την εφαρμογή των παραπάνω ανοσοκυτταροχημικών δεικτών στο υλικό έγκλεισης σε κύβο παραφίνης (cell block) που λαμβάνεται κατά τη διάρκεια της παρακέντησης. Επίσης, η διατήρηση του cell block στο εργαστήριό μας μπορεί να βοηθήσει στην εφαρμογή μελλοντικών, π.χ. μοριακών, τεχνικών.
Ενδείξεις και πλεονεκτήματα της FNA μαστού
Οι κλινικές ενδείξεις της FNA μαστού περιλαμβάνουν:
- τη διάγνωση φλεγμονωδών παθήσεων, πρωτοπαθών νεοπλασμάτων (δ.δ. καλοήθων-κακοήθων αλλοιώσεων), δευτεροπαθών ή μεταστατικών όγκων (συμπεριλαμβανομένων αιματολογικών κακοηθειών), άτυπων επιθηλιακών αλλοιώσεων (απαιτούν περαιτέρω έλεγχο) ή υποτροπής καρκίνου μαστού, και
- τη θεραπεία απλών/φλεγμονωδών κύστεων (εδώ η κένωση της κύστης είναι και θεραπευτική).
Τα πλεονεκτήματα της FNA συνοψίζονται στα παρακάτω:
- Χαμηλό κόστος.
- Είναι ελάχιστα τραυματική τεχνική (οργανικά και ψυχολογικά).
- Είναι καλά αποδεκτή από ιατρούς και ασθενείς.
- Παρέχει γρήγορο και αξιόπιστο αποτέλεσμα (στο νοσοκομείο μας η πρώτη απάντηση δίνεται σε λίγα λεπτά).
- Βοηθά στον προεγχειρητικό σχεδιασμό της θεραπείας.
- Μπορούν να εφαρμοστούν ανοσοκυτταροχημικοί ή μοριακοί δείκτες.
- Εκτιμώνται πολλά οζίδια/αλλοιώσεις.
- Διαφοροδιαγιγνώσκει μαστίτιδα από φλεγμονώδες καρκίνωμα και ενδομαστικούς λεμφαδένες από επιθηλιακές αλλοιώσεις, ιδιαίτερα στην περιοχή της ουράς του μαστού.
- Αποφεύγεται η ανοιχτή βιοψία σε μη νεοπλασματικές αλλοιώσεις, σε ανεγχείρητους ή υποτροπιάζοντες καρκίνους.
- Ανακουφίζει την ασθενή μετά την κενωτική παρακέντηση κύστης.
- Παρέχει ακριβή και γρήγορη εκτίμηση της υποτροπής σε τοπικά αναπτυσσόμενους καρκίνους (ιδίως υποτροπή στο θωρακικό τοίχωμα) για καλύτερη σταδιοποίηση του όγκου.
Οι επιπλοκές της FNA είναι μικρής σημασίας και σχεδόν ανύπαρκτες. Ο πόνος είναι η συχνότερα αναφερόμενη επιπλοκή. Πολύ σπανιότερα έχει επίσης αναφερθεί πνευμοθώρακας.
Άλλες σπάνιες επιπλοκές περιλαμβάνουν αιμορραγία, φλεγμονή. Τέλος σπανιότατα είναι δυνατόν λόγω της FNA να προκύψουν αλλαγές ή artifacts που μπορεί να επηρεάσουν την εκτίμηση των απεικονιστικών (μαστογραφικών) ευρημάτων ή να μιμηθούν διηθητικό καρκίνο στο χειρουργικό παρασκεύασμα. Να τονίσουμε εδώ, όμως, ότι είναι τόσο ασυνήθεις πρακτικά οι επιπλοκές αυτές, που δεν πρέπει να φοβίζουν τις ασθενείς.
Οι σημαντικότεροι περιορισμοί της FNA είναι:
- Δυσκολία στη διάκριση in situ από διηθητικό καρκίνο μαστού.
- Η ακρίβεια συχνά σχετίζεται με το μέγεθος της βλάβης (χαμηλότερη ευαισθησία σε αλλοιώσεις <5mm).
- Χαμηλή ακρίβεια σε όγκους που είναι κυστικοί/νεκρωτικοί, αιμορραγικοί, σε όγκους με δεσμοπλασία ή σε όγκους που βρίσκονται σε μεγάλο βάθος.
- Δεν υπάρχει δυνατότητα για ακριβή τυποποίηση ιδίως καλοήθων αλλοιώσεων.
- Ανάγκη για ανοιχτή βιοψία όγκων των λεγόμενων άτυπων (γκρίζων) διαγνώσεων.
Η αξιολόγηση των ευρημάτων
Ποια είναι όμως τα στοιχεία που αναγνωρίζονται στο μικροσκόπιο σε μια φυσιολογική FNA μαστού και ποια είναι τα γενικά κυτταρολογικά κριτήρια για τον καρκίνο του μαστού;
Στην περίπτωση που πρόκειται για φυσιολογικό μαστό, ο κυτταρολόγος αναγνωρίζει λίγες ομάδες αδενικών κυττάρων με ομοιόμορφους, ομαλούς πυρήνες, ομαλή χρωματίνη, μικρό – δυσδιάκριτο πυρήνιο. Οι ομάδες εμφανίζουν καλή συνοχή και δεν παρατηρείται συνωστισμός ή αλληλεπικάλυψη. Επίσης, αναγνωρίζονται μυοεπιθηλιακά κύτταρα τόσο ανάμεσα στις ομάδες όσο και στο υπόστρωμα. Στο τελευταίο παρατηρούνται ακόμα μακροφάγα, καθώς και μεσεγχυματογενή στοιχεία (συνδετικολιπώδη ιστοτεμαχίδια).
Αντίθετα, στις περιπτώσεις καρκίνου μαστού ο κυτταρολόγος αναγνωρίζει γενικά και ειδικά χαρακτηριστικά κακοήθειας. Στα πρώτα περιλαμβάνονται: μεγάλη κυτταροβρίθεια, αύξηση του μεγέθους των κυττάρων, υψηλή αναλογία πυρήνα-κυτταροπλάσματος, υπερχρωμασία του πυρήνα, μακροπυρήνια, κυτταρικός/πυρηνικός μονομορφισμός, έκκεντρη θέση του πυρήνα, διάσπαση συνοχής – παρουσία μεμονωμένων επιθηλιακών κυττάρων, μιτώσεις, κυτταρικός συνωστισμός και αλληλεπικάλυψη, απουσία μυοεπιθηλίων, νέκρωση.
Στα ειδικά χαρακτηριστικά συγκεκριμένων τύπων καρκίνου περιλαμβάνονται:
- μικρό μέγεθος κυττάρων με κυτταροπλασματικό κενοτόπιο (είναι ένδειξη λοβιακού καρκίνου),
- πλειόμορφοι γυμνοί πυρήνες με μακροπυρήνιο (ένδειξη μυελοειδούς καρκίνου),
- παρουσία άφθονης βλέννης (ένδειξη βλεννώδους καρκίνου),
- παρουσία σωληνίσκων (ένδειξη σωληνώδους καρκινώματος).
Στη συνέχεια, εφόσον ο κυτταρολόγος εκτιμήσει προσεχτικά όλες τις κυτταρικές ομάδες των επιχρισμάτων της FNA, συντάσσει την κυτταρολογική έκθεση, η οποία περιλαμβάνει τις παρακάτω κατηγορίες:
- Μη ικανοποιητικό για εκτίμηση δείγμα (π.χ. όταν υπάρχουν λίγα κύτταρα ή υπάρχει άφθονο αίμα/φλεγμονή).
- Αρνητικό για κακοήθη κύτταρα.
- Παρουσία άτυπων κυττάρων (γκρίζα περιοχή).
- Ύποπτο για κακοήθεια.
- Θετικό για κακοήθεια.
Ωστόσο, πρέπει γιατροί και ασθενείες να γνωρίζουν ότι για διάφορους λόγους ακόμα και στα πιο εξειδικευμένα κέντρα αναφέρονται περιστασιακά ψευδώς αρνητικά ή ακόμα σπανιότερα ψευδώς θετικά αποτελέσματα, που όμως δεν αναιρούν το σημαντικό ρόλο της FNA στη διάγνωση ψηλαφητών και μη ψηλαφητών αλλοιώσεων του μαστού.
Σε ποιες περιπτώσεις, λοιπόν, ενδείκνυται να γίνει FNA μαστού όταν πρόκειται για ψηλαφητή αλλοίωση;
Παρακεντώνται ψηλαφητές αλλοιώσεις κλινικού ενδιαφέροντος (ανεξαρτήτως των απεικονιστικών ευρημάτων), μορφώματα που κλινικά δεν εξηγούνται από τη φυσιολογία ή την ανατομία, ιδίως νεαρών γυναικών, και παρατηρούνται σε 2 μηνιαίους κύκλους, καθώς επίσης και εμμένουσες ή ύποπτες μάζες γυναικών με οικογενειακό ιστορικό (ανεξαρτήτως απεικονιστικών ευρημάτων).
Αναφορικά με τις μη ψηλαφητές αλλοιώσεις μαστού, αυτές παρακεντώνται με τη βοήθεια απεικονιστικών τεχνικών εφόσον είναι ύποπτες για κακοήθεια και απαιτείται συνεκτίμηση κλινικών, απεικονιστικών και κυτταρολογικών ευρημάτων.
Ειδικότερα για τις κύστεις να αναφέρουμε ότι, όταν το υγρό είναι υδαρές, λεπτόρρευστο και δεν παραμένει υπόλειμμα μετά την κενωτική παρακέντηση, τότε αυτό μπορεί είτε να απορριφθεί είτε να αποσταλεί για κυτταρολογική εξέταση. Όταν όμως παραμένει υπολειμματικό ογκίδιο, απαιτείται επανάληψη της FNA. Επίσης, όταν το υγρό της κύστης είναι καφέ/κόκκινο (αιματηρό) πρέπει οπωσδήποτε να αποστέλλεται στο κυτταρολογικό εργαστήριο.
Η σημασία της FNA
Η FNA μπορεί να έχει σημασία στην αντιμετώπιση του καρκίνου του μαστού. Για τη θεραπεία ασθενών με διηθητικό καρκίνο δύο σημαντικά ερωτήματα πρέπει να απαντηθούν σχετικά με τη χορήγηση συμπληρωματικής θεραπείας: υπάρχει όφελος (σημαντικά μεγαλύτερο από τον κίνδυνο) από τη χρησιμοποίηση οποιασδήποτε συμπληρωματικής θεραπείας και ποιος συγκεκριμένος τύπος θεραπείας θα ελαττώσει τον κίνδυνο υποτροπής ή θανάτου της ασθενούς;
Αν και γενικά η ιστολογική εκτίμηση του μεγέθους του όγκου, της διαφοροποίησης και της διήθησης ή μη λεμφαδένων καθορίζει την πρόγνωση, είναι γνωστή και η σημασία μοριακών δεικτών που επηρεάζουν την πρόγνωση και την ανταπόκριση ή όχι στη συστηματική συμπληρωματική θεραπεία.
Οι σημαντικότεροι βιολογικοί δείκτες που προσδιορίζονται σε ιστολογικό υλικό, αλλά και στο υλικό της FNA σε τοπικά αναπτυσσόμενα καρκινώματα και πραγματοποιούνται και στο δικό μας εργαστήριο περιλαμβάνουν:
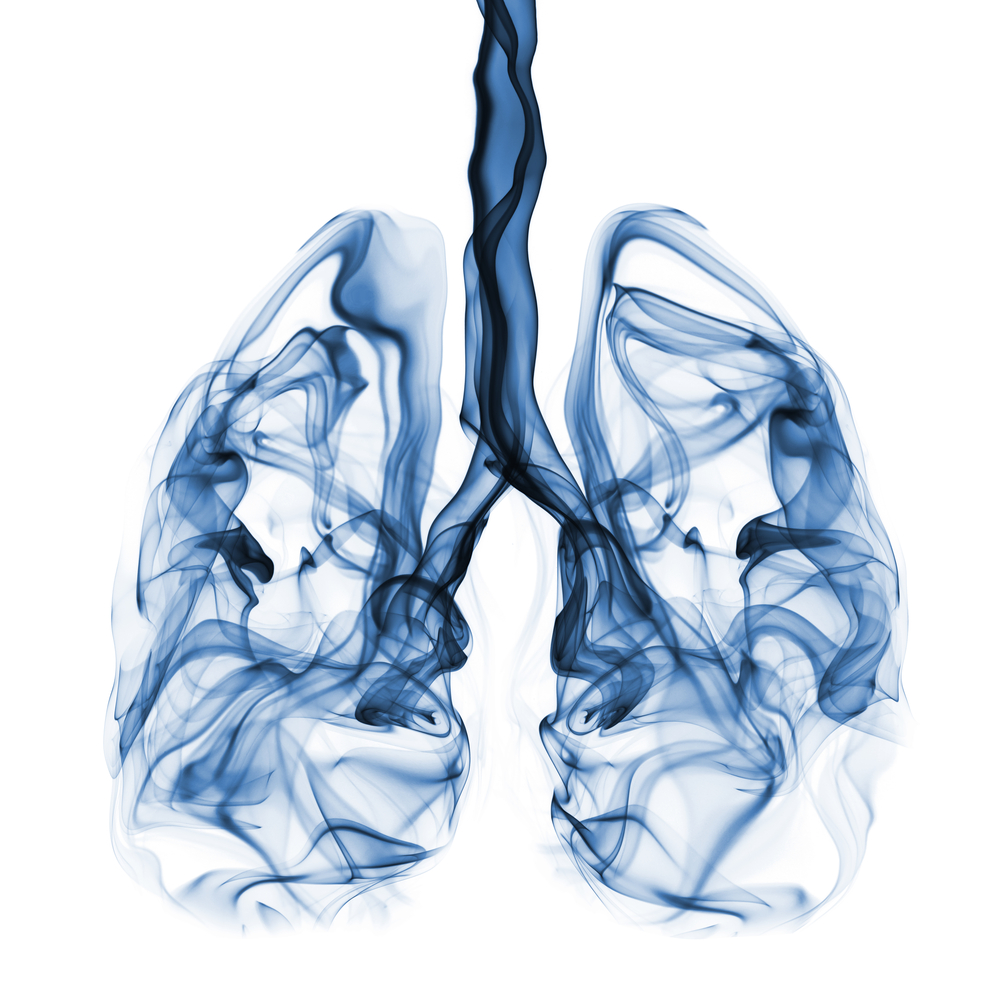
- Οιστρογονικούς και προγεστερονικούς υποδοχείς: Εφαρμόζονται σε όλα τα πρωτοπαθή διηθητικά καρκινώματα για να προβλεφθεί η ανταπόκρισή τους σε ορμονική θεραπεία, π.χ. ταμοξιφαίνη, αναστολείς αρωματάσης κ.ά. (εικόνα 1).
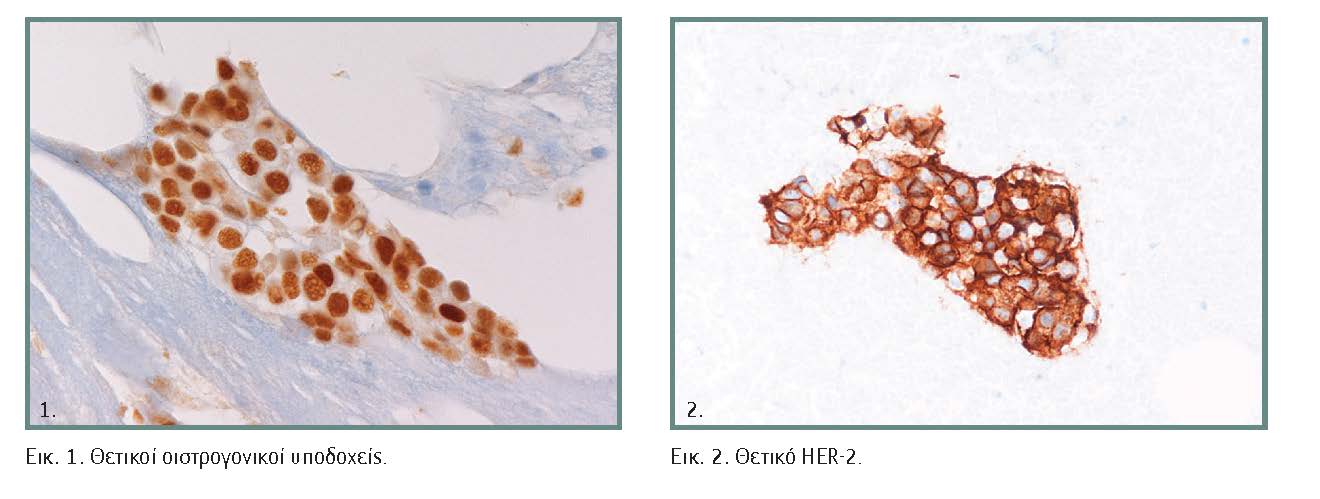
- Πρωτοογκογονίδιο HER-2/neu: Η έκφρασή του σχετίζεται με μικρότερο διάστημα ελεύθερο νόσου, καθώς και με μικρότερη συνολικά επιβίωση της ασθενούς. Επίσης καθορίζει την ανταπόκριση στη στοχευμένη θεραπεία π.χ. Trastuzumab (εικόνα 2).
- Δείκτες πολλαπλασιασμού, π.χ. Ki-67: Υψηλός δείκτης σχετίζεται με προχωρημένο ιστολογικό στάδιο, απουσία ορμονικών υποδοχέων, μεγαλύτερο μέγεθος όγκου και διήθηση λεμφαδένων. Χρησιμοποιείται σε ασθενείς με «αμφίβολη» πρόγνωση, για να καθορίσει εκείνες που έχουν υψηλό κίνδυνο υποτροπής ή θανάτου και δυνητικά θα ωφεληθούν από συμπληρωματική θεραπεία.
- p53: Αδρανοποίηση του ογκοκατασταλτικού αυτού γονιδίου σχετίζεται με κακή πρόγνωση. Επιπλέον η υπερέκφραση p53 μπορεί να υποδηλώνει ανταπόκριση σε συγκεκριμένα χημειοθεραπευτικά, χωρίς να υπάρχουν ακόμα επαρκή βιβλιογραφικά δεδομένα.
Θεωρητικά αναφέρεται ότι και άλλοι δείκτες μπορούν να εφαρμοστούν σε κυτταρολογικό υλικό FNA μαστού, όπως E-cadherin (η έκφραση της οποίας φαίνεται να χάνεται σε λοβιακούς καρκίνους) ή ακόμα και τεχνικές μοριακής βιολογίας, π.χ. southern blot, FISH, mRNA ανάλυση κ.ά. για να αναδείξουν μεταλλάξεις γονιδίων που εμπλέκονται στον καρκίνο του μαστού.
Αξίζει επιπλέον να σημειωθεί και η αξία της παρακέντησης, εκτός των αλλοιώσεων του μαστού, και αυτής των λεμφαδένων, ιδίως απομακρυσμένων, που όταν είναι διηθημένοι καθιστούν τον καρκίνο του μαστού ανεγχείρητο.
Συνοψίζοντας, η FNA μαστού είναι μια σημαντική εξέταση κυρίως για τη διάγνωση, αλλά και για την αντιμετώπιση ψηλαφητών και μη αλλοιώσεων του μαστού, σε συνδυασμό με την κλινική εξέταση και τα απεικονιστικά ευρήματα (triple test). Σε πιστοποιημένα κέντρα, όπως στο δικό μας Νοσοκομείο, είναι ασφαλής μέθοδος, καλά ανεκτή από τις ασθενείς, χαμηλού κόστους και παρέχει γρήγορα και αξιόπιστα αποτελέσματα. Επιπλέον, παρέχει υλικό για περαιτέρω ανοσοκυτταροχημική εκτίμηση προγνωστικών δεικτών ή μοριακή ανάλυση.
Bιβλιογραφία
1. Ali S, Parwani A. Breast Cytopathology. Springer 2007.
2. O?Malley F, Pinder S. Breast Pathology. Churchill Livingstone 2006.
3. Zakhour H, Wells C. Diagnostic Cytopathology of the breast. Churchill Livingstone 1999.
4. Sloaue J. Biopsy Pathology of the breast. Arnold 2001.
5. Romero Q, Bendahl PO, Klintman M, et al. ki67 proliferation in core biopsies versus surgical samples-a model For neo-adjuvant breast cancer studies. BMC Cancer 2011; 11: 341.
6. Hammond ME, Hayes DF, Dowsett M, et al. American Society of Clinical oncology / College of American Pathologists guideline recommendations for immunohistochemical testing of estrogen and progesterone receptors in breast cancer. J Clin Oncol 2010; Jun 1, 28 (16): 2.784-2.795.
Οκτώβριος 2016