Καρδιακή αιτιολογία της κολπικής μαρμαρυγής
Η κολπική μαρμαρυγή είναι μια μορφή υπερκοιλιακής ταχυκαρδίας, η οποία χαρακτηρίζεται από ασύγχρονη κολπική δραστηριότητα με ταυτόχρονη επιδείνωση της μηχανικής δραστηριότητας των κόλπων.
Γράφει ο
Δημήτριος Ευσταθίου
Καρδιολόγος, ΥΓΕΙΑ
Αποτελεί μία από τις συχνότερες αρρυθμίες που απασχολούν το γενικό πληθυσμό και συναντάται ελαφρώς συχνότερα στους άνδρες από ό,τι στις γυναίκες. Η συχνότητά της κυμαίνεται από 1%-2%, ενώ εμφανίζει θετική συσχέτιση με την ηλικία, με αποτέλεσμα στα άτομα άνω των 80 ετών να ανέρχεται σε ποσοστό 10%-15%. Πάνω από 6 εκατομμύρια Ευρωπαίοι πάσχουν από τη συγκεκριμένη αρρυθμία και η επίπτωσή της υπολογίζεται ότι θα διπλασιαστεί τα επόμενα 50 χρόνια, καθώς η μέση ηλικία του πληθυσμού της Ευρώπης συνεχώς αυξάνεται.
Η κολπική μαρμαρυγή ουσιαστικά χαρακτηρίζεται από ασυστολία των κόλπων, κατά την οποία η φυσιολογική κολπική διέγερση καταργείται και υποκαθίσταται από μικρά ακανόνιστα επάρματα, τα μαρμαρυγικά κύματα. Ο χαώδης ρυθμός της και τα χαρακτηριστικά μαρμαρυγικά κύματα πιστεύεται ότι προέρχονται από πολλαπλά μικροκυκλώματα επανεισόδου του ερεθίσματος, εντοπισμένα κυρίως στον αριστερό κόλπο, τα οποία εκπολώνονται σε εξαιρετικά υψηλές συχνότητες.
Η κολπική μαρμαρυγή μπορεί να είναι πρωτοδιαγνωσθείσα, παροξυσμική, εμμένουσα ή χρόνια. Τα αίτιά της ταξινομούνται σε δύο βασικές κατηγορίες, στα καρδιακά ή μη, με τα πρώτα να συναντώνται σε μεγαλύτερη συχνότερα (πίνακας 1).
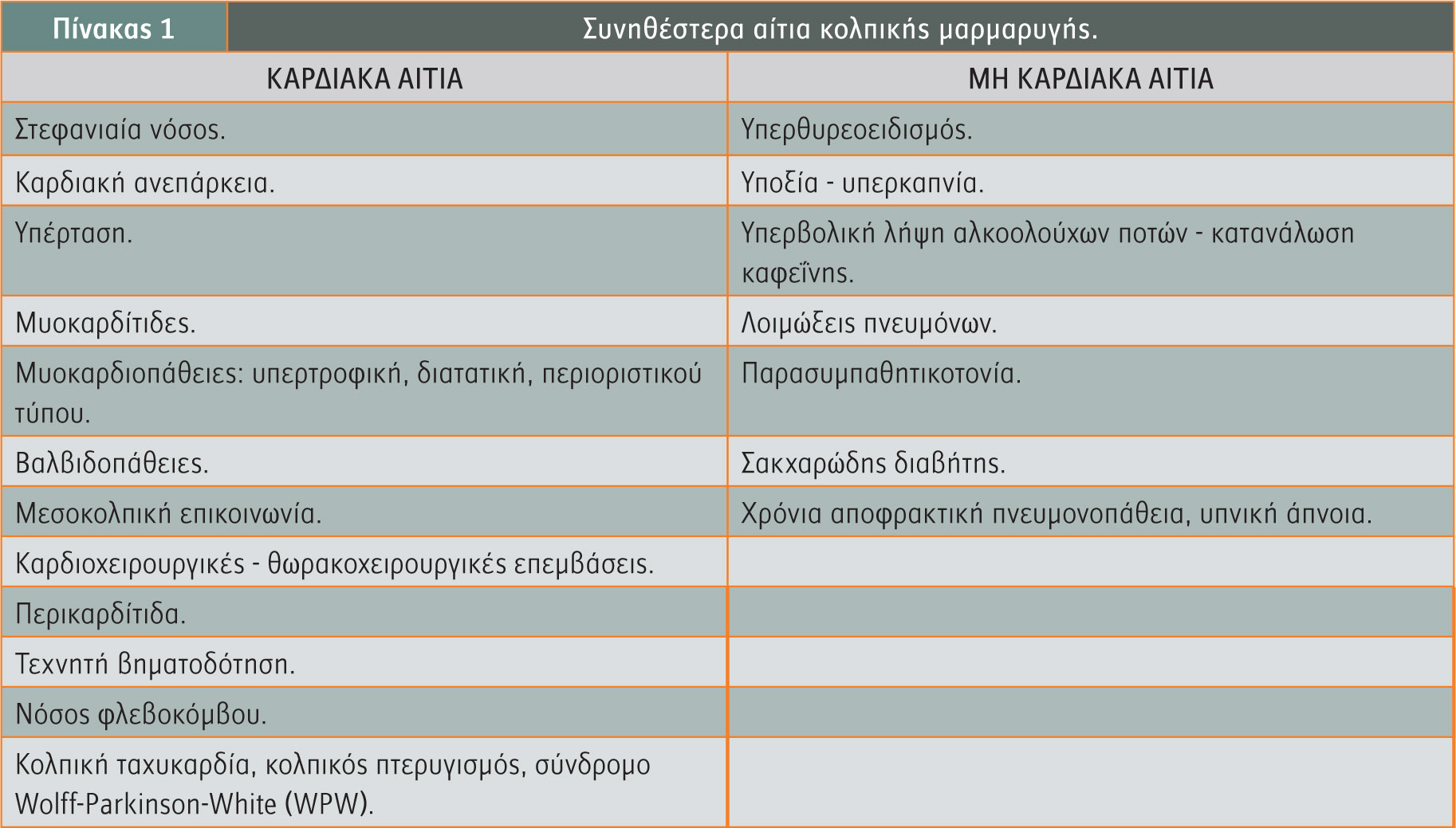
Στο περίπου 15%-20% των ασθενών με κολπική μαρμαρυγή δεν ανιχνεύεται η υποκείμενη αιτία, ενώ σε ορισμένες περιπτώσεις δύναται να σχετίζεται με γενετική προδιάθεση.
Οι κλινικές εκδηλώσεις της κολπικής μαρμαρυγής εξαρτώνται από την κοιλιακή συχνότητα, από τη γενικότερη καρδιακή λειτουργία, καθώς και από τις συνυπάρχουσες παθολογικές καταστάσεις. Η πλειονότητα των ασθενών αναφέρει αίσθημα παλμών, προσυγκοπτικά επεισόδια, ζάλη, καταβολή και δύσπνοια. Λίγοι ασθενείς είναι ασυμπτωματικοί και η διάγνωση της κολπικής μαρμαρυγής είναι τυχαίο εύρημα. Αιμοδυναμικές συνέπειες της κολπικής μαρμαρυγής είναι η απώλεια της κολπικής συστολής και της απώτερης συμμετοχής της στη διατήρηση της καρδιακής παροχής, και η ταχεία κοιλιακή συχνότητα με την επακόλουθη ανεπαρκή πλήρωση των κοιλιών που οδηγεί σε περαιτέρω ελάττωση της καρδιακής παροχής καθώς και σε μείωση της στεφανιαίας αιμάτωσης.
Αναλυτικότερα τα καρδιακά αίτια της κολπικής μαρμαρυγής είναι:
1. Στεφανιαία νόσος: Περίπου το 1/5 των ατόμων με κολπική μαρμαρυγή πάσχει από στεφανιαία νόσο. Δεν έχει πλήρως αποσαφηνισθεί ο μηχανισμός μέσω του οποίου η μη επιπλεγμένη στεφανιαία νόσος (ισχαιμία του κόλπου) προδιαθέτει σε κολπική μαρμαρυγή και με ποιον τρόπο η κολπική μαρμαρυγή αλληλεπιδρά με τη στεφανιαία αιμάτωση.
2. Καρδιακή ανεπάρκεια: Περίπου το 1/3 των ασθενών με κολπική μαρμαρυγή εμφανίζει συμπτωματική καρδιακή ανεπάρκεια σταδίων II-IV κατά NYHA. Η καρδιακή ανεπάρκεια μπορεί να αποτελεί αίτιο ή αποτέλεσμα της αρρυθμίας και μπορεί να οδηγήσει στην εμφάνισή της, μέσω αύξησης της πίεσης και του όγκου του κόλπου και δευτερογενώς μέσω βαλβιδικής δυσλειτουργίας ή χρόνιας νευροχυμικής διέγερσης.
3. Υπέρταση: Η υπέρταση αποτελεί παράγοντα κινδύνου για την εκδήλωση κολπικής μαρμαρυγής και για τις σχετιζόμενες με αυτήν επιπλοκές (αγγειακό εγκεφαλικό επεισόδιο και θρομβοεμβολικά επεισόδια). Σύμφωνα με τη Manitoba Follow-up μελέτη η πιθανότητα εκδήλωσης κολπικής μαρμαρυγής αυξάνεται κατά 1,42 φορά σε άνδρες με ιστορικό αρτηριακής υπέρτασης σε σχέση με άνδρες χωρίς υπέρταση. Το αντίστοιχο ποσοστό επίπτωσης της αρρυθμίας στη συγκεκριμένη πληθυσμιακή ομάδα ήταν 7,5%, εμφανίζοντας θετική συσχέτιση με την ηλικία. Η επίπτωση ήταν μικρότερη από 0,5% στα άτομα κάτω των 50 ετών, φθάνοντας το 9,7% στους άνδρες άνω των 70 ετών. Θα πρέπει να σημειωθεί ότι στα υπερτασικά άτομα η μάζα της αριστερής κοιλίας (υπερτροφία της αριστεράς κοιλίας), η ηλικία και οι διαστάσεις του αριστερού κόλπου είναι ανεξάρτητοι προγνωστικοί παράγοντες για την εκδήλωση της κολπικής μαρμαρυγής.
4. Βαλβιδοπάθειες: Περίπου το 30% των ασθενών με κολπική μαρμαρυγή πάσχει από βαλβιδοπάθεια. Οι ρευματικής αιτιολογίας βαλβιδοπάθειες έχουν μειωθεί τις τελευταίες δεκαετίες λόγω της ευρείας χρήσης αντιβιοτικών και συγκεκριμένα έναντι του υπεύθυνου για το ρευματικό πυρετό β-αιμολυτικού στρεπτόκοκκου της ομάδας Α. Στα αρχικά στάδια της στένωσης ή της ανεπάρκειας της μιτροειδούς βαλβίδας η διάταση του αριστερού κόλπου μπορεί να οδηγήσει σε εμφάνιση κολπικής μαρμαρυγής. Αντίθετα, η αρρυθμία αυτή συναντάται σε μεταγενέστερα στάδια της αορτικής βαλβιδοπάθειας.
5. Μυοκαρδιοπάθειες: Οι μυοκαρδιοπάθειες συνδέονται με αυξημένο κίνδυνο εμφάνισης κολπικής μαρμαρυγής, ιδιαίτερα σε άτομα νεαρής ηλικίας. Μυοκαρδιοπάθεια συναντάται κατά προσέγγιση στο 10% των ασθενών με κολπική μαρμαρυγή.
6. Καρδιοχειρουργικές επεμβάσεις: Στις επεμβάσεις αυτές η πιθανότητα εμφάνισης κολπικής μαρμαρυγής στη μετεγχειρητική περίοδο ανέρχεται στο 30%.
Bιβλιογραφία
1. Stewart S, Hart CL, Hole DJ, McMurray JJ. Population prevalence, incidence, and predictors of atrial fibrillation in the Renfrew/Paisley study. Heart 2001; 86:516-521.
2. Kirchhof P, Auricchio A, Bax J, et al. Outcome parameters for trials in atrial fibrillation: executive summary. Recommendations from a consensus conference organized by the German Atrial Fibrillation Competence NETwork (AFNET) and the European Heart Rhythm Association (EHRA). Eur Heart J 2007; 28:2.803-2.817.
3. Krahn AD, Manfreda J, Tate RB, et al. The natural history of atrial fibrillation: incidence, risk factors and prognosis in the Manitoba Follow-up Study. Am J Med 1995; 98:476-484.
4. Chen YH, Xu SJ, Bendahhou S, et al. KCNQ1 gain-of-function mutation in familial atrial fibrillation. Science 2003; 299:251-254.
5. Levy S, Maarek M, Coumel P, et al. Characterization of different subsets of atrial fibrillation in general practice in France: the ALFA study. The College of French Cardiologists. Circulation 1999; 99:3.028-3.035.
6. Healey JS, Parkash R, Pollak T, et al. CCS Atrial Fibrillation Guidelines Committee. Canadian Cardiovascular Society atrial fibrillation guidelines 2010: etiology and initial investigations. Can J Cardiol. 2011; 27:31-37.
7. Goette A, Bukowska A, Dobrev D, et al. Acute atrial tachyarrhythmia induces angiotensin II type 1 receptor-mediated oxidative stress and microvascular flow abnormalities in the ventricles. Eur Heart J 2009; 30:1.411-1.420.
8. Haissaguerre M, Jais P, Shah DC, et al. Spontaneous initiation of atrial fibrillation by ectopic beats originating in the pulmonary veins. N Engl J Med 1998; 339:659-666.
9. Tsai CF, Tai CT, Hsieh MH, et al. Initiation of atrial fibrillation by ectopic beats originating from the superior vena cava: electrophysiological characteristics and results of radiofrequency ablation. Circulation 2000; 102:67-74.
10. Hsu LF, Jais P, Keane D, et al. Atrial fibrillation originating from persistent left superior vena cava. Circulation 2004; 109:828-832.
11. Bettoni M, Zimmermann M. Autonomic tone variations before the onset of paroxysmal atrial fibrillation. Circulation 2002; 105:2.753-2.759.
Απρίλιος 2012