Κλινική σημασία των μικροαποτιτανώσεων – Βιοψία έπειτα από εντοπισμό με συρμάτινο οδηγό
Οι μικροαποτιτανώσεις αποτελούν ένα από τα συχνότερα μαστογραφικά ευρήματα και σχετίζονται συνήθως με καλοήθεις αιτίες.
Γράφει η
Φιλιώ Μπάδρα MD, PhD
Ακτινολόγος, Τμήμα Μαστογραφίας ΥΓΕΙΑ
Πρόκειται για εναποθέσεις αλάτων ασβεστίου στο μαστό, που είναι ορατές σαν μικρά στίγματα. Σε μικρό ποσοστό ασθενών σχετίζονται με την ανάπτυξη πορογενούς καρκινώματος in situ (DCIS) και λιγότερο συχνά με παρουσία διηθητικού πορογενούς καρκίνου. Σπανιότερα σχετίζονται με λοβιακού τύπου νεοπλασία.
Είναι εξαιρετικής σημασίας ο ρόλος του ακτινολόγου στην αναγνώριση, την εκτίμηση, τη διαφοροδιάγνωση και τελικά το χειρισμό των μικροαποτιτανώσεων, που αποτελούν πολύ συχνό εύρημα του προληπτικού μαστογραφικού ελέγχου (screening mammography). Με βάση τη χημική τους σύσταση οι μικροαποτιτανώσεις ταξινομούνται σε δύο κύριες κατηγορίες: τύπος I, που αποτελείται από οξαλικό ασβέστιο (αφορούν σε καλοήθεις εξεργασίες), και τύπος ΙΙ, που αποτελείται από κρυστάλλους φωσφορικού ασβεστίου (αφορούν σε καλοήθεις ή κακοήθεις εξεργασίες).
Το μέγεθός τους δεν ξεπερνά τα 50-500 μ, γεγονός που καθιστά την αναγνώριση και την εκτίμησή τους πολύ δύσκολη διαδικασία.
Ανατομία
Είναι πολύ χρήσιμη για την κατανόηση της μορφολογίας των αποτιτανώσεων η συσχέτιση του σχήματος και της θέσης τους με τις ανατομικές και τις λειτουργικές δομές του μαστού, καθώς και με τις παθολογικές διεργασίες σε αυτές.
Η βασική λειτουργική μονάδα του μαστού είναι το λοβίδιο-TDLU (Terminal Ductal Lobular Unit).
To λοβίδιο αποτελείται από 10-100 βοτρύδια (acini), που καταλήγουν σ? έναν τελικό πόρο. Ο τελικός πόρος καταλήγει σε μεγαλύτερους πόρους και τελικά στον κύριο πόρο του λοβίου (ή του τμήματος) που εκβάλλει στη θηλή. Το λοβίδιο ως δομή είναι εξαιρετικής σημασίας γιατί οι περισσότερες νεοπλασίες ξεκινούν από εκεί.
Αποτελεί τη θέση ανάπτυξης του πορογενούς καρκινώματος in situ (DCIS), του λοβιακού καρκινώματος in situ (LCIS), καθώς και καλοήθων καταστάσεων όπως η ινοκυστική αλλαγή, η αδένωση, η υπερπλασία και η επιθηλίωση. Η πλειονότητα των αποτιτανώσεων αναπτύσσεται εντός των τελικών πόρων (ενδοπορικές-intraductal) ή εντός των βοτρυδίων (λοβιακού τύπου-lobular) (εικόνες 1 και 2).
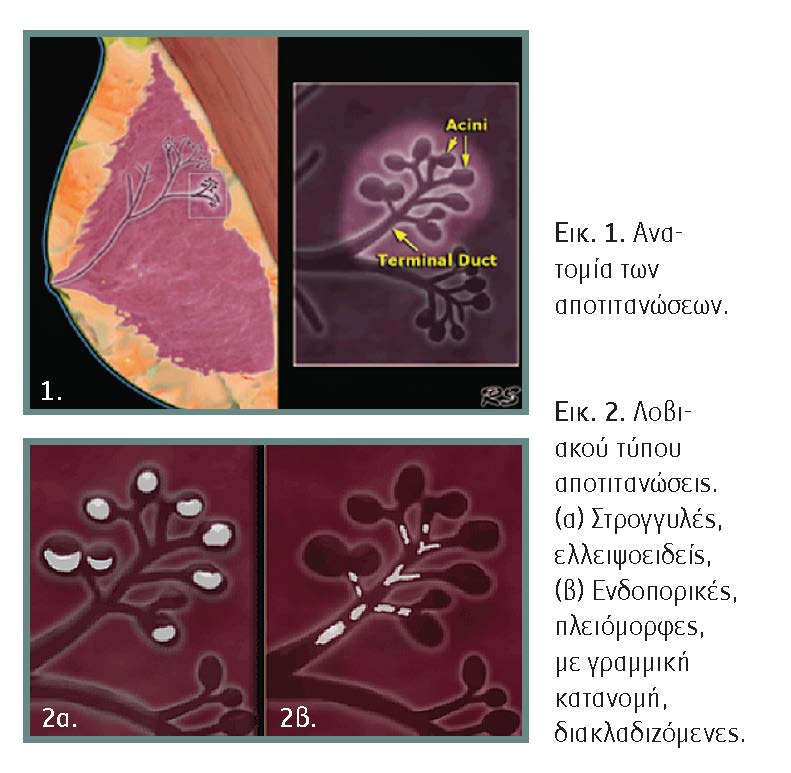
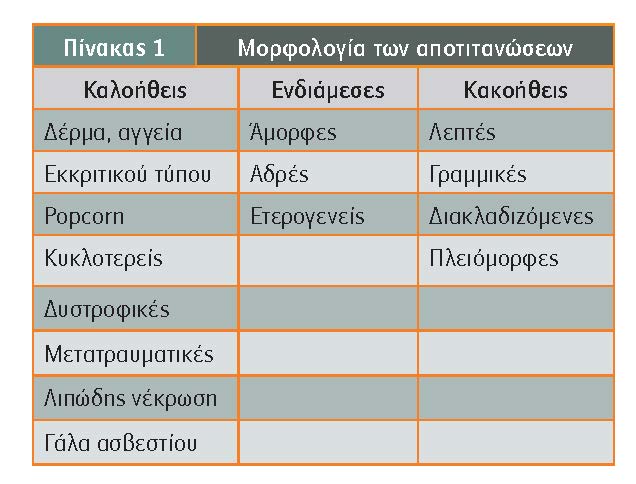
- Λοβιακού τύπου αποτιτανώσεις: Πληρούν τα βοτρύδια, που συχνά είναι διατεταμένα. Είναι ομοιογενείς, στρογγυλές ή ελλειψοειδείς, καλά περιγεγραμμένες. Όταν συνυπάρχει βαθμός ίνωσης, μπορεί να είναι μικρότερου μεγέθους και πιο ανομοιογενείς, δύσκολα διακριτές από τις ενδοπορικές. Συνήθως είναι διάσπαρτες, όπως και η διαδικασία που τις προκαλεί, και καλοήθεις.
- Ενδοπορικές αποτιτανώσεις: Οφείλονται στην ασβεστοποίηση εκκρίσεων ή κυτταρικού υλικού εντός των πόρων. Είναι ανομοιογενείς ως προς το σχήμα, το μέγεθος και την πυκνότητά τους (πλειόμορφες). Πολλές φορές μπορεί να αποτελούν εκμαγείο του πόρου με χαρακτηριστική διακλαδιζόμενη, γραμμική μορφολογία. Είναι ύποπτες για ανάπτυξη κακοήθειας.
Διαγνωστική προσπέλαση
Η διαγνωστική προσπέλαση των μικροαποτιτανώσεων βασίζεται στην εκτίμηση της μορφολογίας τους, που είναι και το κυριότερο κριτήριο, της κατανομής τους και της μεταβολής τους στην πορεία του χρόνου.
Μορφολογία: Είναι το βασικότερο κριτήριο που χρησιμοποιείται για τη διαφοροδιάγνωση των μικροαποτιτανώσεων. Αν δεν είναι δυνατό να χαρακτηριστούν τυπικά καλοήθεις ή κακοήθεις, χαρακτηρίζονται «ενδιάμεσης υποψίας» (πίνακας 1).
Κατανομή:
- Διάσπαρτες: Εκτείνονται σε όλο το μαζικό αδένα.
- Περιοχικές: Σε περιοχή >2 cc, αλλά όχι κατά μήκος πόρου.
- Συρρέουσες: Περισσότερες από 5 σε αριθμό, σε έκταση 1 cm2.
- Τμηματικές: Σε κατανομή πόρου που αφορά σε λόβιο ή τμήμα.
Μεταβολή στο χρόνο: Η απεικονιστική τους σταθερότητα στο χρόνο δεν εξασφαλίζει απαραίτητα και την καλοήθη φύση τους, αντιθέτως η εμφάνιση νέων αποτιτανώσεων με ενδιάμεσα μορφολογικά χαρακτηριστικά θέτει υποψία για την ανάπτυξη κακοήθειας (εικόνα 3).
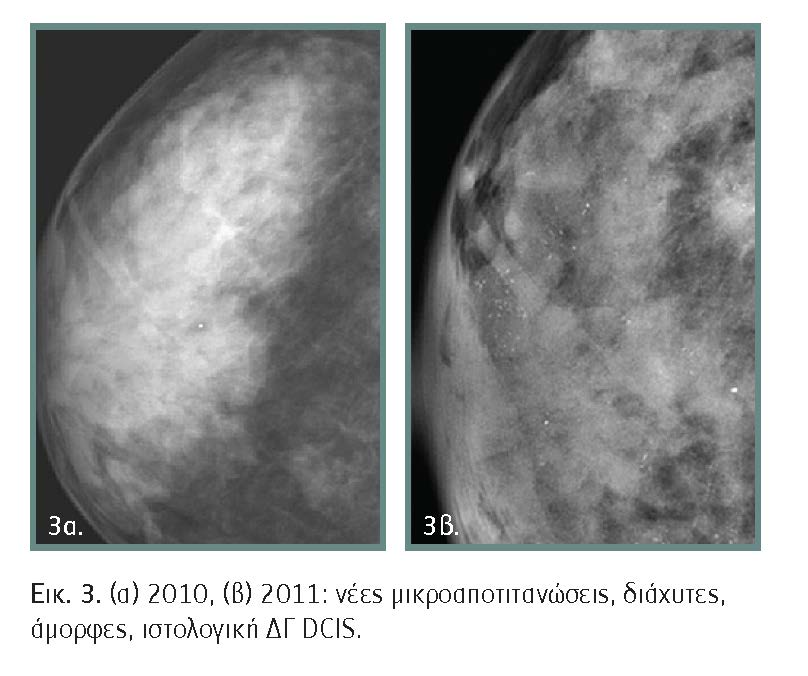
Καλοήθεις αποτιτανώσεις
- Δερματικού τύπου: Είναι στρογγυλές με διαυγαστικό κέντρο, μπορεί να είναι διάχυτες ή να σχετίζονται με σπίλους. Η χρήση ταλκ στο δέρμα μπορεί να μιμηθεί την παρουσία αποτιτανώσεων.
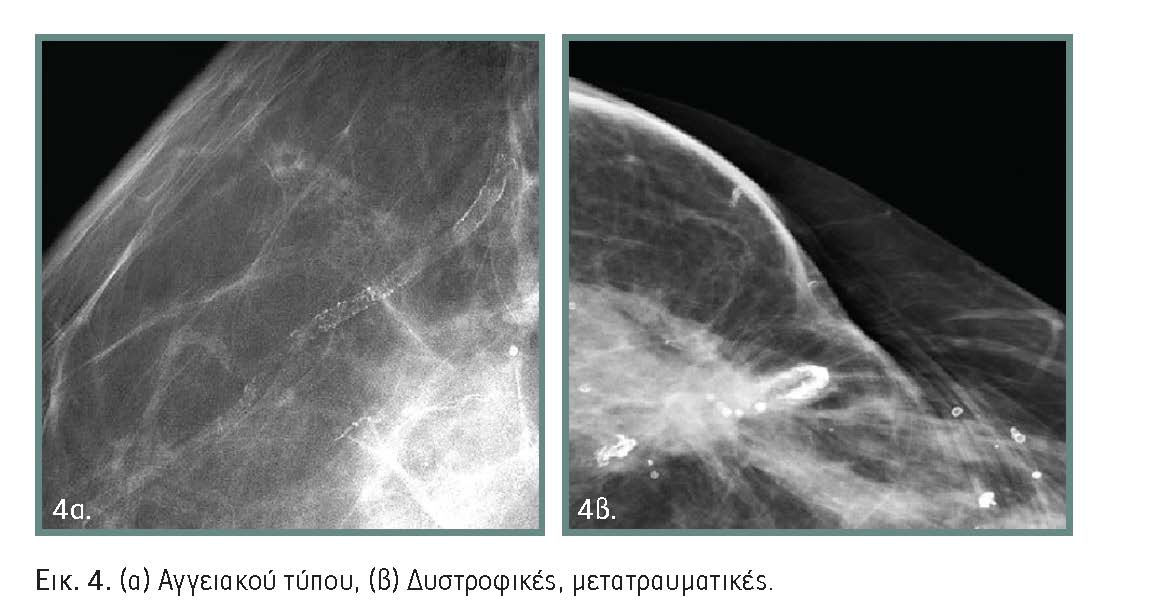
- Αγγειακού τύπου: Είναι γραμμοειδείς και παράλληλες (tram track-line), πιο συχνές σε μεταεμμηνοπαυσιακές ασθενείς (σχετίζονται με αθηρωματική νόσο) ή σε νεαρότερες με διαβήτη.
- Δυστροφικoύ τύπου: Αναπτύσσονται σε ουλώδη ιστό, είναι αδρές με ακανόνιστο σχήμα και μπορεί να σχετίζονται με τραύμα, αιμάτωμα, χειρουργική επέμβαση, ακτινοθεραπεία, φλεγμονώδη ή μεταβολική νόσο, καθώς επίσης να αναπτύσσονται στην επιφάνεια εμφυτευμάτων (εικόνα 4).
- Εκκριτικού τύπου: Αναπτύσσονται κατά μήκος των πόρων, είναι κυλινδρικές και σχετίζονται με εκτασία των πόρων, περιπορική μαστίτιδα, εκκριτική νόσο, πλασματοκυτταρική μαστίτιδα.
- Λοβιακού τύπου: Εντός της τελικής ανατομικής δομής του βοτρυδίου, είναι στρογγυλές, ελλειψοειδείς, ίσως σχηματίζουν ομάδες, μπορεί να είναι διάσπαρτες ή συρρέουσες και συχνά είναι δύσκολο να διαφοροδιαγνωστούν από κακοήθεις.
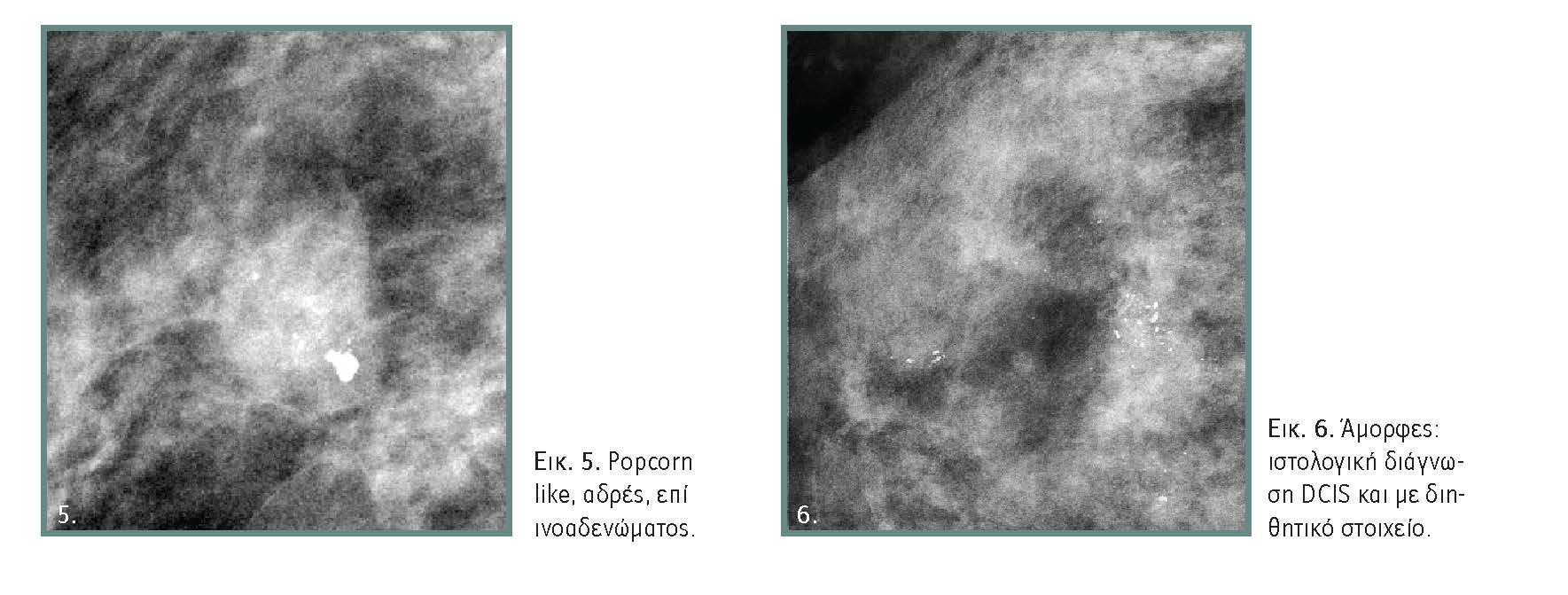
- Αδρές (coarse), χαρακτηριστικές Cpopcorn likeE: αυτές που αναπτύσσονται επί ινοαδενωμάτων, κυκλοτερείς, αυτές που αφορούν σε τοιχώματα κύστεων (εικόνα 5).
Αποτιτανώσεις ενδιάμεσης υποψίας για ανάπτυξη κακοήθειας
Εάν οι μικροαποτιτανώσεις δεν εμφανίζουν τυπικά καλοήθη μορφολογία, τότε χαρακτηρίζονται ύποπτες για την ανάπτυξη κακοήθειας. Αυτές συνήθως είναι άμορφες ή αδρές ετερογενείς. Συνήθως αυτές είναι εκείνες που επιλέγονται για βιοψία, η οποία θέτει και την ακριβή διάγνωση.
- Άμορφες: Είναι αυτές που δεν έχουν σαφές σχήμα και τύπο. Συνήθως είναι μικρές, με ασαφή μορφολογία, που δεν επιτρέπει τη μορφολογική τους ταξινόμηση. Με τέτοιου είδους αποτιτανώσεις μπορεί να εμφανίζονται τόσο καλοήθεις όσο και κακοήθεις καταστάσεις (εικόνα 6).
- Αδρές ετερογενείς: Είναι >0,5 cm, με ανώμαλο σχήμα και μπορεί να υποδηλώνουν τόσο καλοήθη όσο και κακοήθη αιτιολογία. Η ΔΔΓ τους περιλαμβάνει:
- Ινοαδένωμα.
- Ίνωση.
- Μετατραυματική βλάβη, συμπεριλαμβανομένης της λιπώδους νέκρωσης.
- DCIS.
Αποτιτανώσεις υψηλής πιθανότητας για κακοήθεια
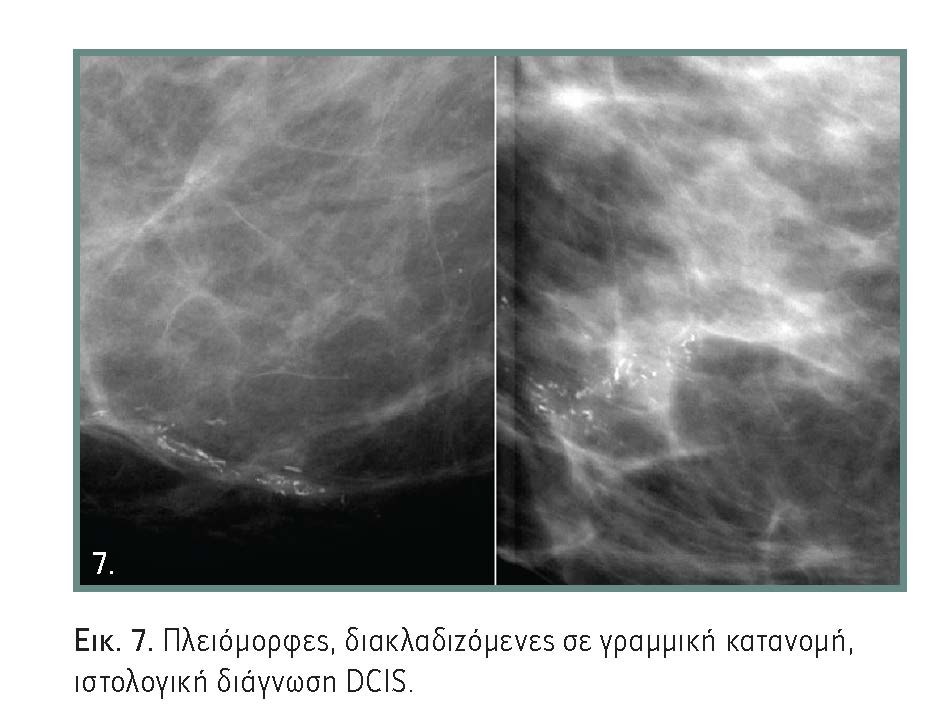
Είναι λεπτές, πλειόμορφες, ανομοιογενείς ως προς την πυκνότητά τους και το σχήμα τους, και γραμμικές, διακλαδιζόμενες. Αναπτύσσονται κατά μήκος πόρου ή με τμηματική κατανομή και συνήθως χαρακτηρίζουν τα high-grade DCIS (εικόνα 7).
Artifacts
Artifacts όπως δακτυλικά αποτυπώματα, σκόνη στο εμφανιστήριο, τρίχες, δερματοστιξία, χρήση καλλυντικών στο δέρμα, αποσμητικά και καλλυντικά στο δέρμα του μαστού μπορούν να μιμηθούν την παρουσία μικροαποτιτανώσεων.
Χειρουργική βιοψία μαστού – Προεγχειρητικός εντοπισμός με βελόνη υπό μαστογραφική καθοδήγηση
Από τη στιγμή που οι μικροαποτιτανώσεις θεωρηθούν ύποπτες και ζητηθεί ιστολογική ταυτοποίηση της αλλοίωσης, υπάρχουν διαθέσιμες διάφορες μέθοδοι.
Η επιλογή της μεθόδου που θα χρησιμοποιηθεί εξαρτάται από πολλούς παράγοντες συμπεριλαμβανομένων του μεγέθους της βλάβης, του εντοπισμού της και των μορφολογικών και απεικονιστικών χαρακτηριστικών της. Καθεμία από τις μεθόδους έχει πλεονεκτήματα και μειονεκτήματα που εκτιμώνται σε κάθε περίπτωση.
Η χειρουργική βιοψία των μικροαποτιτανώσεων είναι μια τεχνική που πραγματοποιείται σε δύο βήματα. Σε πρώτη φάση γίνεται ο προεγχειρητικός εντοπισμός υπό την καθοδήγηση του μαστογράφου (εφόσον δεν συνυπάρχει ψηλαφητικό εύρημα) και στη συνέχεια η ασθενής οδηγείται στο χειρουργείο για την εξαίρεση της περιοχής που έχει σημανθεί.
Ο εντοπισμός περιλαμβάνει την τοποθέτηση ενός συρμάτινου οδηγού στην περιοχή ενδιαφέροντος, ο οποίος παραμένει και αφαιρείται από το χειρουργό μαζί με την περιοχή-στόχο. Η τοποθέτηση γίνεται από τον ακτινολόγο με μια απλή και καλά ανεκτή διαδικασία. Αρχικά, έπειτα από ήπια αντισηψία του δέρματος, ο μαστός συμπιέζεται με ειδικό βαθμονομημένο πίεστρο και επιλέγεται ο στόχος. Η καθοδήγηση της βελόνας-οδηγού γίνεται από το γιατρό και στη συνέχεια λαμβάνονται λήψεις για την επιβεβαίωση της θέσης της.
Αφού επιβεβαιωθεί ότι βρίσκεται στο σωστό σημείο, απελευθερώνεται μέσα από τον αυλό της ο συρμάτινος οδηγός, ο οποίος φέρει ένα άγκιστρο στο άκρο του, που τον ακινητοποιεί στο εύρημα και δεν επιτρέπει τη μετακίνηση του στο εξής. Η όλη διαδικασία χρονικά δεν ξεπερνά συνήθως τα 20-30 λεπτά.
Η ασθενής στη συνέχεια οδηγείται στο χειρουργείο και ο χειρουργός αφαιρεί το τμήμα του ιστού που βρίσκεται γύρω από τον οδηγό. Το τμήμα αυτό αποστέλλεται στο μαστογράφο και ακτινογραφείται για να επιβεβαιωθεί η εξαίρεση των αποτιτανώσεων. Ο ακτινολόγος εκτιμά αν η εξαίρεση είναι ικανοποιητική και επικοινωνεί με το χειρουργό, ο οποίος ολοκληρώνει την επέμβαση. Αν εκτιμηθεί ότι η εξαίρεση δεν είναι επαρκής, μπορεί να ζητηθεί να γίνει ευρύτερη εκτομή έως ότου επιτευχθούν υγιή όρια (εικόνα 8).
Το κύριο πλεονέκτημα της μεθόδου έναντι των άλλων διαδερμικών τεχνικών που χρησιμοποιούνται, είναι η σχεδόν 100% ακρίβεια στη διάγνωση, δεδομένου ότι εξαιρείται όλη η περιοχή ενδιαφέροντος και γι? αυτό προτείνεται ειδικά για τις μικροαποτιτανώσεις υψηλής πιθανότητας για κακοήθεια, για τις οποίες μπορεί να αποτελέσει και την τελική χειρουργική θεραπεία, χωρίς δηλαδή να απαιτηθεί νέα επέμβαση.
Κλινική σημασία των μκροαποτιτανώσεων
Η συχνότητα διάγνωσης του πορογενούς καρκινώματος in situ (DCIS) έχει αυξηθεί δραματικά μέσα στα τελευταία 15 έτη. Έχει αλλάξει επίσης τα τελευταία χρόνια ο τρόπος εμφάνισης της νόσου, από ψηλαφητή μάζα, έκκριμα θηλής ή νόσο Paget της θηλής σε σιωπηρές κλινικά βλάβες, μαστογραφικά διαγνώσιμες.
Το πιο συχνό μαστογραφικό εύρημα που σχετίζεται με την ανάπτυξη πορογενούς καρκινώματος in situ (DCIS) είναι η παρουσία μικροαποτιτανώσεων σε ασυμπτωματικές γυναίκες. Με τη διαρκή βελτίωση των διαθέσιμων απεικονιστικών τεχνικών και την ευρύτερη συμμετοχή των γυναικών στα προγράμματα πληθυσμιακού ελέγχου, σήμερα το DCIS αντιπροσωπεύει το 22%-45% όλων των διαγνωσθέντων καρκίνων του μαστού.
Με την αύξηση της συχνότητας διάγνωσης προέκυψαν αντικρουόμενες απόψεις στη διεθνή βιβλιογραφία, που αφορούν στη βιολογική σπουδαιότητα αυτού του τύπου των αλλοιώσεων. Το βέβαιο είναι ότι πρόκειται για μια ιδιαίτερα ετερογενή ομάδα τόσο ως προς τα μαστογραφικά, κλινικά και ιστολογικά χαρακτηριστικά της όσο και ως προς την εν γένει βιολογική της συμπεριφορά. Μερικοί τύποι μπορεί να εξελίσσονται ταχύτατα σε διηθητική νόσο, ενώ άλλοι να μην εξελιχθούν ποτέ.
Ο προβληματισμός που παραμένει είναι αν υπάρχουν πραγματικά κριτήρια διάκρισης αυτών ακριβώς των αλλοιώσεων με δυναμικό εξέλιξης σε διηθητική νόσο και πρόβλεψης της χρονικής στιγμής που αυτό θα γίνει, από αυτές που θα παρέμεναν κλινικά σιωπηρές. Το ερώτημα αυτό παραμένει αναπάντητο, όπως και το αν τελικά γίνεται υπερδιάγνωση (overdiagnosis) της νόσου και εφαρμόζονται θεραπείες που δεν είναι πραγματικά αναγκαίες (overtreatment-υπερθεραπεία).
Φαίνεται ότι η μορφολογία των μικροαποτιτανώσεων έχει κάποια σχέση με την εξέλιξη, με τις υψηλής πιθανότητας για κακοήθεια αποτιτανώσεις να χαρακτηρίζουν τα high-grade DCIS, αυτά δηλαδή με υψηλό δυναμικό εξέλιξης σε διηθητική νόσο, και τις ενδιάμεσης πιθανότητας για κακοήθεια, άμορφες, να χαρακτηρίζουν μια εξελικτική διαδικασία από την άτυπη επιθηλιακή υπερπλασία ως τα low–grade DCIS, με χαμηλότερο δυναμικό εξέλιξης σε διηθητική νόσο.
Στη διεθνή βιβλιογραφία αναφέρονται προσπάθειες συσχέτισης βιολογικών προγνωστικών δεικτών των νεοπλασμάτων με τη μαστογραφική απεικόνιση των μικροαποτιτανώσεών τους, με σκοπό την καλύτερη επιλογή θεραπείας για την κάθε περίπτωση. Το βέβαιο είναι πως, παρότι μπορεί να γίνεται υπερδιάγνωση και υπερθεραπεία σε κάποιες περιπτώσεις, η πρώιμη διάγνωση και η θεραπεία είναι κομβικές, δεδομένου ότι το DCIS με τη σωστή αντιμετώπιση θεωρείται ιάσιμη νόσος με άριστη πρόγνωση.
Bιβλιογραφία
1. Feig S. Breast imaging,categorical course in diagnostic radiology. RSNA syllabus 2005.
2. The benefits and harms of breast cancer screening: an independent review. The Lancet, Nov 2012; 9855 (380): 1.778-1.786.
3. Ernst MF, et al. Wire localization of non-palpable breast lesions, out of date? Breast 2002, Oct; 11: 408-413.
4. de Paredes ES, Langer TG, Cousins J. Interventional breast procedures. Cur. Prob. Diagn. Radiol. 1998, Oct; 27: 133-184.
5. Gisvold, et al. Breast biopsy: A comparative Study of Stereotaxically Guided Core and Excisional Techniques. AJR 1994; 162: 815-820.
6. Smithuis R, Pijnappael R. Differential Diagnosis of Breast Calcifications. The radiology assistant 2008, May.
7. American college of radiology. Breast imaging reporting and data system (BI-RADS): breast imaging atlas. 4th ed Reston, Va; American college of radiology 2003.
Οκτώβριος 2016








































