Ο μύθος της χημειοπροφύλαξης στις υποτροπιάζουσες λοιμώξεις του ουροποιητικού στα παιδιά
Η λοίμωξη του ουροποιητικού (ΛΟ) θεωρείται μία από τις πιο συχνές βακτηριακές λοιμώξεις τόσο στα νήπια όσο και στα παιδιά σχολικής ηλικίας.
Γράφει ο
Σωτήριος Μπόγρης
Χειρουργός – Ουρολόγος Παίδων/Εφήβων
Παίδων ΜΗΤΕΡΑ
Επιδημιολογικές μελέτες σε διαφορετικούς πληθυσμούς έδειξαν ότι το 3% – 7% των θήλεων και το 1% – 2% των αρρένων θα νοσήσουν τουλάχιστον μία φορά μέχρι την ηλικία των 6 ετών. Το ποσοστό εμφάνισης νέας λοίμωξης ουροποιητικού σε διάστημα 12 μηνών από το πρώτο επεισόδιο κυμαίνεται από 12% έως 30%.
Σύμφωνα με το National Institute of Clinical Excellence (NICE) 2007, ως υποτροπιάζουσες λοιμώξεις ουροποιητικού (ΥΛΟ) ορίζονται οι ακόλουθες περιπτώσεις:
- Δύο ή περισσότερα επεισόδια λοίμωξης ανώτερου ουροποιητικού/οξείας πυελονεφρίτιδας (ΟΠ).
- Ένα επεισόδιο ΟΠ και ένα ή περισσότερα επεισόδια λοίμωξης κατώτερου ουροποιητικού (ΛΚΟ).
- Τρία ή περισσότερα επεισόδια ΛΚΟ.
Οι παράγοντες κινδύνου για τις ΥΛΟ, όπως αυτοί διατυπώθηκαν σε μια τελευταία ανασκόπηση Cochrane του 2011, είναι: η κυστεοουρητηρική παλινδρόμηση (ΚΟΠ), η ασταθής ουροδόχος κύστη (νευρογενής ή μη νευρογενής) και, τέλος, η προηγούμενη ΛΟ (με φυσιολογικό ουροποιητικό ή με προγεννητική υδρονέφρωση). Επίσης, φάνηκε ότι το φύλο είναι καθοριστικός παράγοντας, αφού τα κορίτσια εμφανίζουν πιο συχνά υποτροπές από ό,τι τα αγόρια.
Το Esch. Coli είναι ο υπεύθυνος παθογόνος μικροοργανισμός στο 80% των περιστατικών.
Ο χρυσός κανόνας για την αντιμετώπιση και τη θεραπεία των ΥΛΟ, και που ως πρακτική χρησιμοποιείται ακόμη και σήμερα, είναι η χορήγηση αντιμικροβιακής προφύλαξης ή αλλιώς χημειοπροφύλαξης (ΧΜΦ). Η χρήση της ΧΜΦ, όμως, στηρίζεται περισσότερο σε μελέτες του 1970, οι οποίες σήμερα αξιολογούνται με πολύ χαμηλό επίπεδο ιατρικής τεκμηρίωσης (Evidence Based Medicine – L 5) και χωρίς στατιστική ανάλυση τις περισσότερες φορές. Οι τυχαιοποιημένες μελέτες που δημοσιεύτηκαν γι? αυτό το θέμα τη δεκαετία του 1970 ήταν μόλις 5, ενώ από το 2006 έως το 2011 έχουν δημοσιευτεί περίπου 10, στις οποίες συγκαταλέγονται 3 μετααναλύσεις και 2 συστηματικές ανασκοπήσεις. Η ΧΜΦ, σύμφωνα με τις οδηγίες από το Βασιλικό Ιατρικό Κολέγιο του Λονδίνου του 1991, θα έπρεπε να χορηγείται σε κάθε παιδί ύστερα από το πρώτο επεισόδιο λοίμωξης έως ότου γίνει διερεύνηση για υποκείμενη πάθηση, αλλά και σε ασυμπτωματική βακτηριουρία. Με αυτές της οδηγίες συμφωνούσε και η Αμερικανική Εταιρεία Παιδιατρικής. Το 2007 το Εθνικό Ινστιτούτο Υγείας της Μεγάλης Βρετανίας (NICE 2007 Guidelines for UTI In Children) εξέδωσε νέες οδηγίες για τη χρήση της ΧΜΦ.
Σύμφωνα με αυτές:
- ΧΜΦ δεν θα πρέπει να προτείνεται σε νεογνά και παιδιά μετά το πρώτο επεισόδιο ΛΟ.
- Ίσως να θεωρείται κατάλληλη θεραπεία σε νεογνά και παιδιά με ΥΛΟ.
- Σε ασυμπτωματική βακτηριουρία δεν θα πρέπει να χορηγείται ΧΜΦ σε νεογνά και παιδιά.
Ακόμη και σήμερα χρειάζεται να καθοριστεί με ευκρίνεια ο ρόλος της ΧΜΦ στην αντιμετώπιση των ΥΛΟ στα παιδιά. Δυστυχώς, η χρήση της δεν είναι αθώα, όπως ήδη αποδεικνύεται και το σημαντικότερο μειονέκτημα είναι η ανάπτυξη ανθεκτικών στελεχών σε κοινά αντιβιοτικά. Εξάλλου, η συμμόρφωση των ασθενών στη ΧΜΦ είναι θέμα που δεν έχει διερευνηθεί πλήρως από καμία μελέτη, αφήνοντας ερωτήματα σχετικά με την αποτελεσματικότητά της όταν αυτή χρησιμοποιείται περιστασιακά ή διακόπτεται για διάστημα μεγαλύτερο των δύο μηνών και, κατά συνέπεια, με τη δημιουργία πολύ ανθεκτικών μικροβίων.
Η ΧΜΦ είχε σκοπό να μειώσει το ποσοστό υποτροπών, ό,τι αυτό συνεπάγεται, δηλαδή μείωση των νεφρικών ουλών, μικρότερα ποσοστά εμφάνισης αρτηριακής υπέρτασης στο μέλλον και μειωμένα ποσοστά ασθενών με νεφρική νόσο τελικού σταδίου (ESRF).
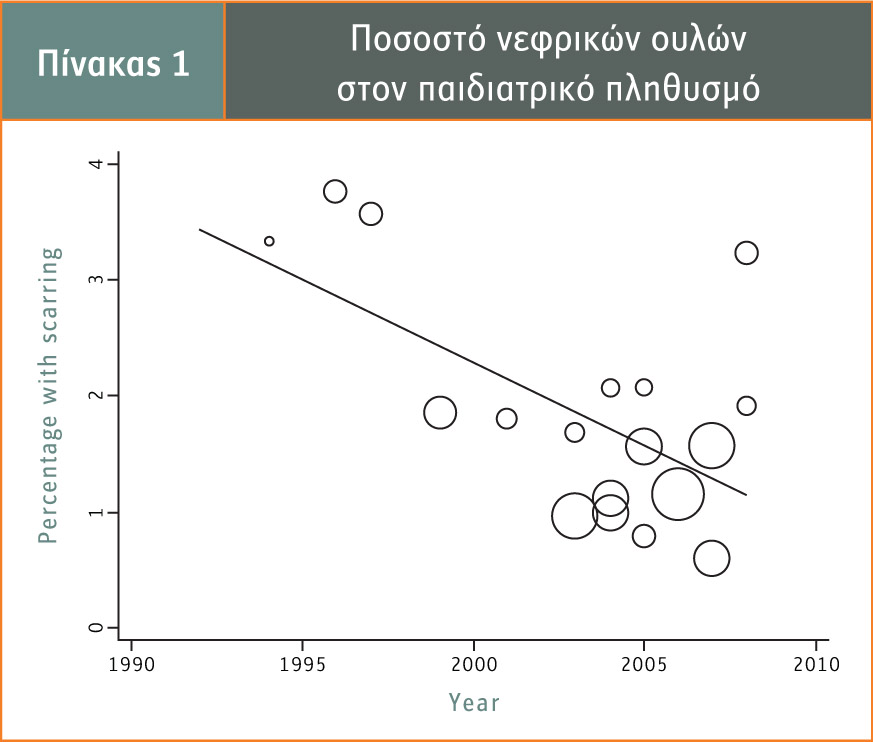
Όσον αφορά στις νεφρικές βλάβες, ο Shaikh et al. σε μια συστηματική ανασκόπηση του 2011 ανέφερε ότι το 15% των παιδιών μετά το πρώτο επεισόδιο ΛΟ εμφάνισε νεφρική βλάβη στο DMSA από 5 έως 24 μήνες αργότερα. Από παλαιότερες μελέτες, παροδική και μόνιμη νεφρική βλάβη εμφάνιζαν αντίστοιχα το 40% και το 5% των παιδιών με ΥΛΟ. Σύμφωνα με τον Shaikh, οι νεφρικές ουλές υπερεκτιμώνταν από παλαιότερες μελέτες και σε αυτό βοηθούσε το γεγονός πως δεν ξεχώριζαν αρχικά τους εκ γενετής δυσπλαστικούς νεφρούς, με αποτέλεσμα τα ποσοστά των νεφρικών βλαβών να είναι υψηλότερα. Η παραπάνω συστηματική ανασκόπηση έδειξε ότι το ποσοστό των νεφρικών ουλών στον παιδιατρικό πληθυσμό μειώνεται σε συνάρτηση με το έτος της μελέτης (πίνακας 1).
Η ΧΜΦ κατέχει σήμερα σημαντική θέση στην αντιμετώπιση της κυστεοουρητηρικής παλινδρόμησης (ΚΟΠ). Το ποσοστό των παιδιών με ΥΛΟ που πάσχουν από ΚΟΠ είναι 30% – 40%. Σήμερα, οι απόψεις για τη χρήση της ενάντια στις ΥΛΟ από ΚΟΠ χαμηλού βαθμού (Ι-ΙΙΙ) είναι αντικρουόμενες. Στην παρούσα ανασκόπηση δεν θα γίνει αναφορά για τις ΥΛΟ από ΚΟΠ, καθώς και αυτοί οι ασθενείς αποτελούν ιδιαίτερη κατηγορία.
Η συζήτηση θα περιοριστεί σε δύο άλλες μεγάλες κατηγορίες ασθενών:
Α. Στα παιδιά με ΥΛΟ και φυσιολογικό ουροποιητικό.
Β. Στα παιδιά με ιστορικό προγεννητικής διάγνωσης υδρονέφρωσης.
Α. Παιδιά με ΥΛΟ και φυσιολογικό ουροποιητικό
Από τις μελέτες που ασχολήθηκαν με τον ρόλο της ΧΜΦ σε παιδιά με ΥΛΟ και φυσιολογικό ουροποιητικό ξεχωρίζει αυτή του Conway et al. σε 75.000 παιδιά, η οποία έδειξε ότι η ΧΜΦ όχι μόνο δεν μείωσε την εμφάνιση υποτροπών, αλλά συσχετίστηκε και με την αύξηση των επιπέδων αντιμικροβιακής αντίστασης. Η μελέτη του Craig et al. παρακολούθησε 576 παιδιά με περισσότερα από ένα επεισόδια ΛΟ για έναν χρόνο, που τυχαιοποιημένα χωρίστηκαν σε δύο ομάδες, σε αυτά που έλαβαν και σε αυτά που δεν έλαβαν ΧΜΦ. Ο μέσος όρος ηλικίας στη συγκεκριμένη μελέτη ήταν οι 14 μήνες και το συμπέρασμα ήταν ότι η ομάδα αυτών που έλαβαν ΧΜΦ εμφάνισε λιγότερες υποτροπές. Σε αντίθετο συμπέρασμα κατάληξε η τελευταία μεταανάλυση (2011) των Williams και Craig.
Συγκεκριμένα, η ΧΜΦ φαίνεται να μειώνει την εμφάνιση συμπτωματικών ΥΛΟ σε συγκεκριμένες ομάδες παιδιών, χωρίς όμως σαφές πλεονέκτημα, ενώ ταυτόχρονα πρέπει να αντισταθμιστεί ο αυξημένος κίνδυνος αντιμικροβιακής αντίστασης που προκαλεί. Σε παρόμοια μεταανάλυση των Mori et al. η ΧΜΦ δεν κατάφερε να μειώσει το ποσοστό εμφάνισης νεφρικών ουλών, αλλά περιόρισε το ποσοστό ασθενών με μικροβιουρία. Στα μειονεκτήματα των τυχαιοποιημένων μελετών συγκαταλέγονται ο ανεπιτυχής διαχωρισμός σε ομάδες σχετικά με το διαφορετικό επίπεδο εκπαίδευσης της ούρησης στις διάφορες ηλικίες, αλλά και η κατάσταση της ακροποσθίας για τα αγόρια, αφού έχει τεκμηριωθεί ότι η ΧΜΦ δεν καταφέρνει να εξαλείψει τον μικροβιακό πληθυσμό κάτω από την πόσθη.
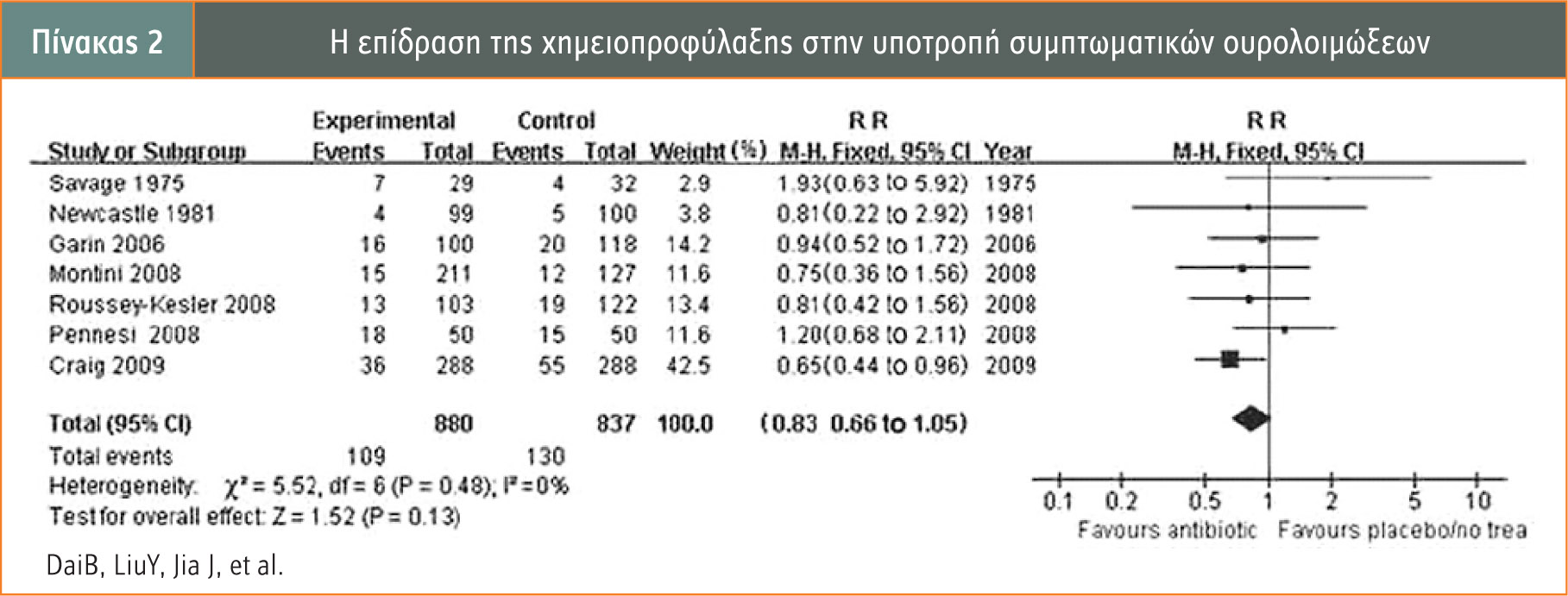
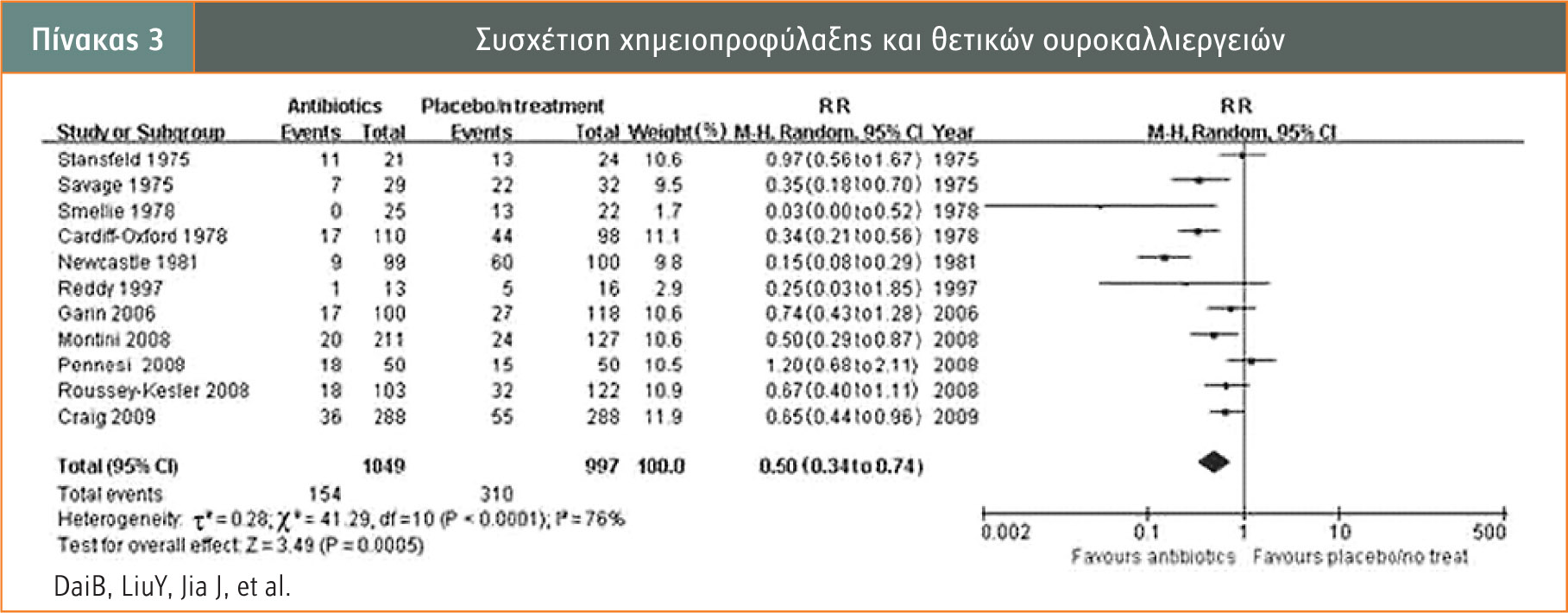
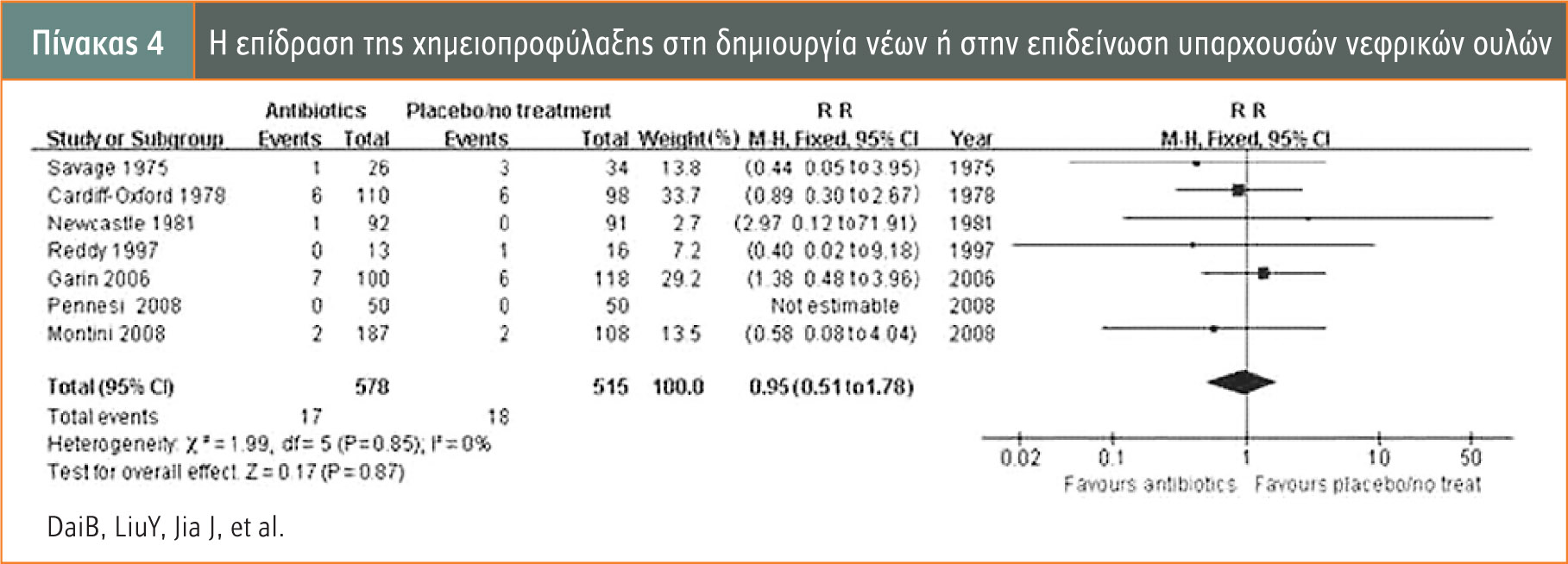
Η συστηματική ανασκόπηση και μεταανάλυση 11 τυχαιοποιημένων μελετών των Bing et al., που δημοσιεύτηκε το 2010, κατέληξε στο συμπέρασμα, απουσία ιατρικής τεκμηρίωσης, ότι η ΧΜΦ μειώνει την εμφάνιση ΥΛΟ στον παιδιατρικό πληθυσμό. Συγκεκριμένα, ο παράγοντας κινδύνου (risk ratio) υπέρ της ΧΜΦ για τη μείωση των ΥΛΟ είναι 0,83% (CI: 95%) (πίνακας 2), αντίστοιχα ο παράγοντας κινδύνου για τη μείωση των θετικών καλλιεργειών είναι 0,5% (CI: 95%) (πίνακας 3) και ο παράγοντας κινδύνου υπέρ της ΧΜΦ για τον ρυθμό ανάπτυξης νέων ή επιδείνωσης των νεφρικών ουλών είναι 0,95% (CI: 95%) (πίνακας 4).
Β. Παιδιά με ιστορικό προγεννητικής διάγνωσης υδρονέφρωσης
Οι μελέτες αξιολόγησης της ΧΜΦ σε παιδιά με ιστορικό προγεννητικής διάγνωσης υδρονέφρωσης αφορούν σε μικρό αριθμό περιστατικών, λόγω όμως της παρακολούθησης κατά τη νεογνική περίοδο κρίνονται επιτυχημένες.
Ως αποτέλεσμα της ανάπτυξης και της χρήσης των προγεννητικών υπερήχων, σήμερα η εμβρυϊκή υδρονέφρωση (ΕΥ) είναι η πιο συχνή ανωμαλία και αφορά στο 1% – 5% των εγκύων. Παρόλη την αυξημένη συχνότητα εμφάνισης, δεν έχει διαμορφωθεί από την παιδοουρολογική κοινότητα κοινή οδηγία για την αντιμετώπιση της ΕΥ μετά τη γέννηση. Από τις πιο συχνές παθήσεις είναι η στένωση της πυελοουρητηρικής και της κυστεοουρητηρικής συμβολής, που προκαλεί όμως μερική απόφραξη και κατά κανόνα υποχωρεί αυτόματα σε βάθος χρόνου. Τα περισσότερα από αυτά τα παιδιά παρακολουθούνται, χωρίς να υπάρχει ανάγκη για χειρουργική επέμβαση, αντιμετωπίζονται όμως σχεδόν στο σύνολό τους με τη χορήγηση ΧΜΦ για μεγάλα χρονικά διαστήματα.
Ο Lee et al. σε μια πρόσφατη έρευνα παρακολούθησε 430 νεογνά με ιστορικό ΕΥ για 1 έτος χωρίς ΧΜΦ. Μέσα σε 6 μήνες νόσησε με ΛΟ το 19% αυτών γι? αυτό και κατέληξε στο συμπέρασμα ότι η ΧΜΦ βοήθησε. Στη συγκεκριμένη ομάδα συγκαταλέγονταν παιδιά με ουρητηροκήλες (κλειστές), ενώ παράλληλα δέχτηκαν για τη διάγνωση της ΛΟ και δείγματα ούρων με συλλογή από σακουλάκι, γεγονός που ανέβασε το ποσοστό θετικών καλλιεργειών. Αντίθετα, ο Roth et al. παρακολούθησε 92 παιδιά με ΕΥ 3ου και 4ου βαθμού της Εμβρυϊκής Ουρολογικής Εταιρείας για περίπου 27 μήνες χωρίς ΧΜΦ. Είχαν 4 επεισόδια ΛΟ, τα δύο ήταν κορίτσια και τα άλλα δύο μη περιτετμημένα αγόρια. Φυσικά, το συμπέρασμά τους ήταν κατά της χρήσης της ΧΜΦ σε παιδιά με ιστορικό ΕΥ.
Συνοψίζοντας, ο Creenfield SP σε ανασκόπησή του το 2011 για τον ρόλο της ΧΜΦ στην αντιμετώπιση της ΕΥ, κατέληξε στο συμπέρασμα ότι είναι λογικό να παρακολουθούνται αυτά τα παιδιά χωρίς ΧΜΦ και πως η περιτομή για τα άρρενα νεογνά διαδραματίζει προστατευτικό ρόλο. Το συμπέρασμά του, όμως, για τα νεογνά με ΕΥ άμφω ήταν πως, παρότι δεν υπάρχουν ευκρινείς μελέτες και ενδείξεις με υψηλή ιατρική τεκμηρίωση, θα μπορούσε κάποιος να τα αντιμετωπίσει με ΧΜΦ.
Συνοψίζοντας, θα πρέπει να δίνεται ιδιαίτερη προσοχή στα παιδιά με φυσιολογικό ουροποιητικό όσον αφορά στα αίτια των ΥΛΟ και συγκεκριμένοι παράγοντες κινδύνου όπως η ηλικία, το φύλο, η εκπαίδευση της ούρησης και η κατάσταση της ακροποσθίας για τα αγόρια θα πρέπει να συνεκτιμώνται. Η ιατρική τεκμηρίωση για τη χρήση της ΧΜΦ σε αυτήν την ομάδα είναι αδύναμη. Αναφορικά με την ομάδα των παιδιών με ιστορικό ΕΥ, θεωρείται ότι οι πιθανότητες εμφάνισης ΛΟ στη νεογνική ηλικία είναι λίγες κι αυτό προϋποθέτει ότι η χρήση της ΧΜΦ θα πρέπει να γίνεται επιλεκτικά σε συγκεκριμένους ασθενείς.
Bιβλιογραφία
1. Mahant S, Friedman J, MacArthur C. Renal ultrasound findings and vesicoureteral reflux in children hospitalised with urinary tract infection. Arch Dis Child 2002; 86:419 – 420.
2. Uhari M, Nuutinen M. Epidemiology of symptomatic infections of the urinary tract in children. BMJ 1988; 297:450 – 452.
3. Conway PH, Cnaan A, Zaoutis T, et al. Recurrent urinary tract infections in children: risk factors and association with prophylactic antimicrobials. JAMA 2007; 298:179 – 186.
4. Panaretto K, Craig J, Knight J, et al. Risk factors for recurrent urinary tract infection in preschool children. J Paediatr Child Health 1999; 35:454 – 459.
5. Clinical guidelines CG 54 Clinical Guideline August 2007, National Institute of Clinical Excellence (NICE). Urinary tract infection: diagnosis treatment and long-term management of urinary tract infection in children (http://guidance.nice.org.uk).
6. Williams G, Craig JC. Long-term antibiotics for preventing recurrent urinary tract infection in children (Review). Τhe Cochrane Library 2011, Issue 3.
7. Rushton HG. Urinary tract infections in children. Epidemiology, evaluation and management. Pediatric Clinics of North America. 1997; 44: 1.133 – 1.169.
8. Dai B, Liu Y, Jia J, et al. Long-term antibiotics for the prevention of recurrent urinary tract infection in children: a systematic review and meta-analysis. Arch Dis Child 2010; 95:499 – 508.
9. Guidelines for the management of acute urinary tract infection in childhood. Report of a Working Group of the Research Unit, Royal College of Physicians. Journal of the Royal College of Physicians of London 1991; 25(1).
10. Shaikh Ν, Ewing AL, Bhatnagar S, et al. Risk of Renal Scarring in Children With a First Urinary Tract Infection: A Systematic Review. Pediatrics 2010; 126;1.084 – 1.091.
11. Coulthard MG, Lambert HJ, Keir MJ. Occurrence of renal scars in children after their first referral for urinary tract infection. BMJ. 1997 Oct 11; 315(7113):918 – 919.
12. Craig JC, Irwig LM, Knight JF, et al. Symptomatic urinary tract infection in preschool Australian children. Journal of Paediatrics & Child Health 1998; 34:154 – 159.
13. Craig JC, Simpson JM, Williams GJ, et al. Prevention of recurrent urinary tract in children with vesicoureteric reflux and normal renal tracts (PREVENT Investigators). NEJM 2009; 361:1.748 – 1.759.
14. Mori R, Fitzgerald A, Williams C, et al. Antibiotic prophylaxis for children at risk of developing urinary tract infection: a systemic review. Acta Paed 2009; 98:1.781 – 1.786.
15. Lee RS, Cendron M, Kinnamon DD, et al. Antenatal hydronephrosis as a predictor of postnatal outcome: a meta-analysis. Pediatrics 2006; 118:586 – 593.
16. Roth CC, Hubanks JM, Bright BC, et al. Occurence of urinary tract infection in children with significant upper urinary tract obstruction. Urology 2009; 73:74 – 78.
17. Greenfield SP. Antibiotic Prophylaxis in Pediatric Urology: An Update. Curr Urol Rep 2011; 12:126 – 131.
Νοέμβριος 2011