Ο ρόλος της προγεννητικής διάγνωσης στην αντιμετώπιση των συγγενών χειρουργικών παθήσεων
Ο προγεννητικός έλεγχος στηρίζεται όλο και περισσότερο στην υπερηχογραφική διάγνωση όχι μόνο για την ομαλή ανάπτυξη του εμβρύου, αλλά και για την πρώιμη διάγνωση συγγενών ανωμαλιών.
Γράφει ο
Χάρης Χ. Χηνιάδης
Μαιευτήρας-Χειρουργός Γυναικολόγος, ΜΗΤΕΡΑ & ΥΓΕΙΑ
Η πρόοδος στην τεχνολογία των υπερηχοτομογράφων και η εύκολη πρόσβαση σε γυναικολόγους ειδικευμένους στη μαιευτική υπερηχογραφία έχουν βοηθήσει στη διάγνωση ανωμαλιών ήδη από το υπερηχογράφημα της αυχενικής διαφάνειας του 1ου τριμήνου της κύησης στο πλαίσιο του ελέγχου για το σύνδρομο Down. Ο αναλυτικότερος έλεγχος, όμως, γίνεται αργότερα και είναι πλέον αποδεδειγμένη η χρησιμότητα του υπερηχογραφικού προγεννητικού ελέγχου στο 2ο τρίμηνο της κύησης για τη διάγνωση συγγενών και χρωμωσωμικών ανωμαλιών.
Μεγάλες συγγενείς ανωμαλίες αναφέρονται σε τουλάχιστον 2% όλων των εμβρύων και νεογνών και έχουν σοβαρή επίπτωση στην περιγεννητική και νεογνική νοσηρότητα και θνητότητα. Τις τελευταίες δεκαετίες, με τη χρήση του προγεννητικού υπερηχογραφήματος, η συχνότητα διάγνωσης των συγγενών ανωμαλιών έχει αυξηθεί σημαντικά.
Τα τελευταία χρόνια έχει γίνει συχνότερη η χρήση της μαγνητικής τομογραφίας στον προγεννητικό έλεγχο. Όμως, η επιπλέον χρήση της μαγνητικής τομογραφίας στην προγεννητική διάγνωση των συγγενών χειρουργικών ανωμαλιών του κοιλιακού τοιχώματος, φαίνεται να έχει σημαντικότητα όσον αφορά στη διάγνωση του είδους του ιστού της βλάβης και όχι στη διάγνωση της βλάβης αυτής καθ? εαυτήν, ισχυροποιώντας την αξία του προγεννητικού υπερηχογραφήματος.
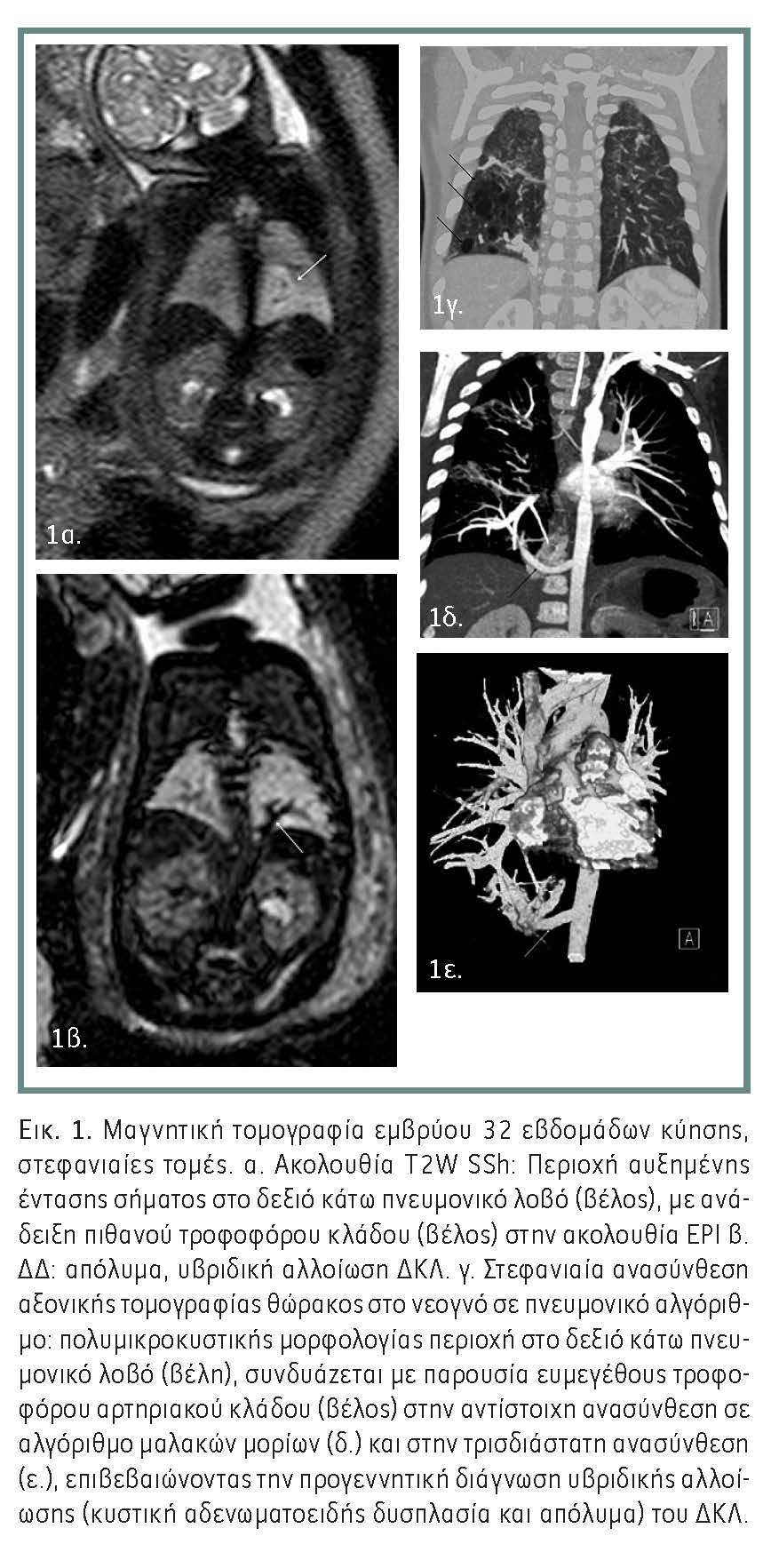
Ο ρόλος της προγεννητικής διάγνωσης είναι να αυξήσει την πιθανότητα να έχει το νεογνό την πρέπουσα παρακολούθηση της κύησης, τη γέννηση σε πλήρη Μαιευτική Μονάδα, τη φροντίδα σε Μονάδα Εντατικής Θεραπείας Νεογνών και το σχεδιασμό της αποκατάστασης της βλάβης μετά τον τοκετό. Σε πανευρωπαϊκό επίπεδο η προγεννητική διάγνωση είναι επιτυχής στο 64% των περιπτώσεων, ενώ το 68% αυτών έγινε πριν από τις 24 εβδομάδες κύησης. Παρ? όλα αυτά μεγάλο ποσοστό εγκύων (43%) επιλέγει τη διακοπή της κύησης μετά την προγεννητική διάγνωση.
Η στατιστική αυτή επιβεβαιώνει πως ακόμα και σε περιπτώσεις όπως η ομφαλοκήλη και η γαστρόσχιση, που μπορεί να είναι μεμονωμένα ευρήματα, η επιλογή της εγκύου είναι -πιο συχνά απ? ότι πρέπει- η διακοπή της κύησης. Αυτό σηματοδοτεί την ανάγκη για πρώιμο, ενδελεχή έλεγχο, αλλά και αναλυτική ενημέρωση των γονέων για το εύρος των περιγεννητικών επιπλοκών και επεμβάσεων.
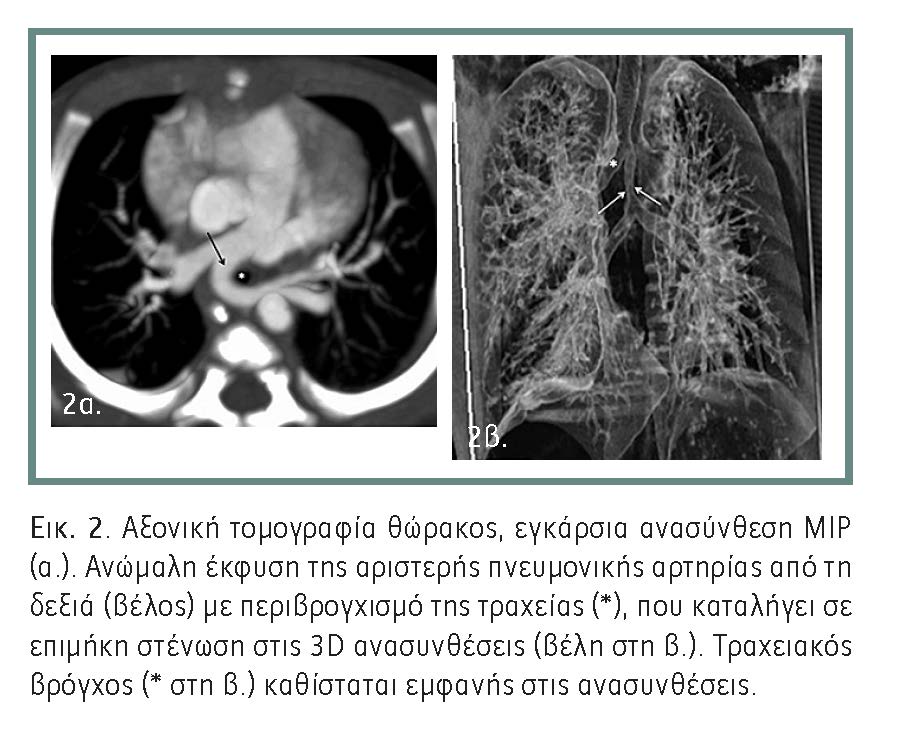
Είναι πλέον αποδεδειγμένο ότι η παρουσία του παιδοχειρουργού και η ενημέρωση τόσο της εγκύου όσο και του μαιευτήρα στο προγεννητικό στάδιο της διάγνωσης, μπορεί να επιφέρουν αλλαγές προς το καλύτερο στις αποφάσεις για διακοπή της κύησης, τον τρόπο, το χρόνο και τον τόπο της γέννησης του παιδιού. Με αυτόν τον τρόπο εξασφαλίζονται οι ιδανικές συνθήκες αντιμετώπισης των χειρουργικών ανωμαλιών και μειώνεται η επίπτωσή τους στην υγεία του νεογνού.
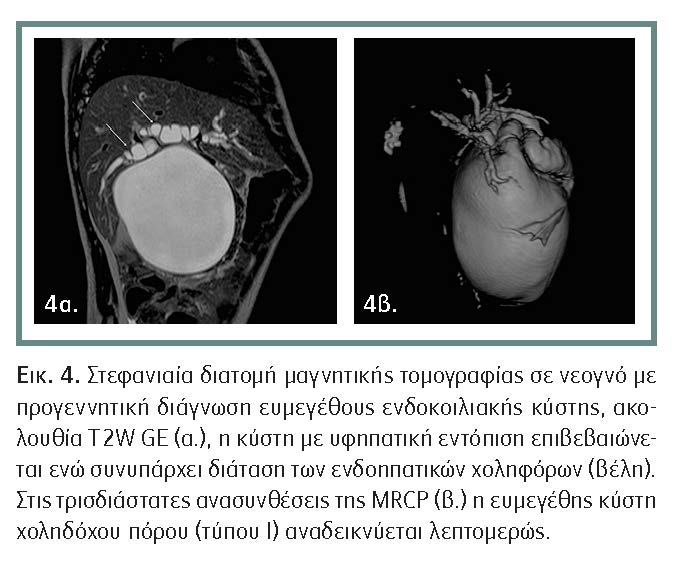
• Κύστη ωοθήκης: Οι συγγενείς κύστες οωθήκης είναι οι πιο συχνά ευρισκόμενες κοιλιακές κύστες και 50% τουλάχιστον από αυτές υποχωρούν αυτόματα είτε πριν είτε μετά τη γέννηση. Στις υπόλοιπες περιπτώσεις είναι συχνή η χειρουργική παροχέτευση ή και η αφαίρεση ολόκληρου του εξαρτήματος εάν κριθεί απαραίτητο λόγω συστροφής ή υποκείμενης παθολογίας.
• Διαφραγματοκήλη: Η συγγενής διαφραγματοκήλη αντιστοιχεί στο 8% όλων των μεγάλων συγγενών ανωμαλιών. Η διάγνωσή της είναι εύκολη, ακόμα και από τη 16η εβδομάδα της κύησης. Η επιλογή του χρόνου γέννησης του νεογνού με διαφραγματοκήλη, φαίνεται να ευνοεί την περίοδο της 37ης εβδομάδας με καισαρική τομή. Παρ? όλα αυτά, φαίνεται πως δεν υπάρχει απόλυτη συμφωνία μεταξύ των μελετητών, με ορισμένους να υποστηρίζουν την περαιτέρω αναμονή προς την 39η-40ή εβδομάδα. Επίσης, παρά την πρόοδο της ιατρικής και της νεογνολογίας, το ποσοστό θνησιμότητας και νοσηρότητας παραμένει υψηλό.
• Ατρησία λεπτού και παχέος εντέρου: Η ατρησία του δωδεκαδακτύλου είναι η συχνότερη αιτία απόφραξης του λεπτού εντέρου. Η προγεννητική διάγνωση είναι συχνή (23%-31%) και έχει στατιστικά σημαντικό ρόλο στο ποσοστό επιβίωσης του νεογνού. Σήμερα η άμεση χειρουργική αντιμετώπιση λόγω της έγκαιρης διάγνωσης με υπερήχους, βοηθά στην άμεση χειρουργική αποκατάσταση της λειτουργικότητας του εντέρου μετά τη γέννηση με υψηλά ποσοστά επιβίωσης (78%-94%).
• Ομφαλοκήλη: Η ομφαλοκήλη, η πιο συχνή ανωμαλία του κοιλιακού τοιχώματος (1:5.000 γεννήσεις) σε ποσοστό μεγαλύτερο του 40% σχετίζεται με επιπλέον συγγενείς και χρωμωσωμικές ανωμαλίες. Παρότι διαγιγνώσκεται προγεννητικά σε ποσοστό μεγαλύτερο του 75%, υπάρχει σημαντική διαφορά στη θνητότητα, που σχετίζεται με το αν είναι παρούσες και επιπλέον ανωμαλίες, χρωμοσωμικές ή μη. Η προγεννητική διάγνωση με επεμβατικό έλεγχο – αμνιοπαρακέντηση/λήψη τροφοβλάστης- βοηθά στη σωστή επιλογή της μητέρας για την πιθανή διακοπή της κύησης ή την πρόοδο της κύησης και τη γέννηση μετά τις 34 εβδομάδες.
• Γαστρόσχιση: Στη γαστρόσχιση η επιλογή του χρόνου γέννησης πρέπει να ισορροπήσει μεταξύ της καθυστέρησης της εντερικής λειτουργίας λόγω της έκθεσης των ελίκων στο αμνιακό υγρό και της προωρότητας του εμβρύου. Η καισαρική τομή πρέπει να γίνεται στο τέλος της 36ης εβδομάδας κύησης ή το αργότερο μέχρι την 38η εβδομάδα. Η άμεση σύγκλιση του κοιλιακού τοιχώματος μετά τη γέννηση έχει σημαντική αξία στην μείωση της νοσηρότητας.
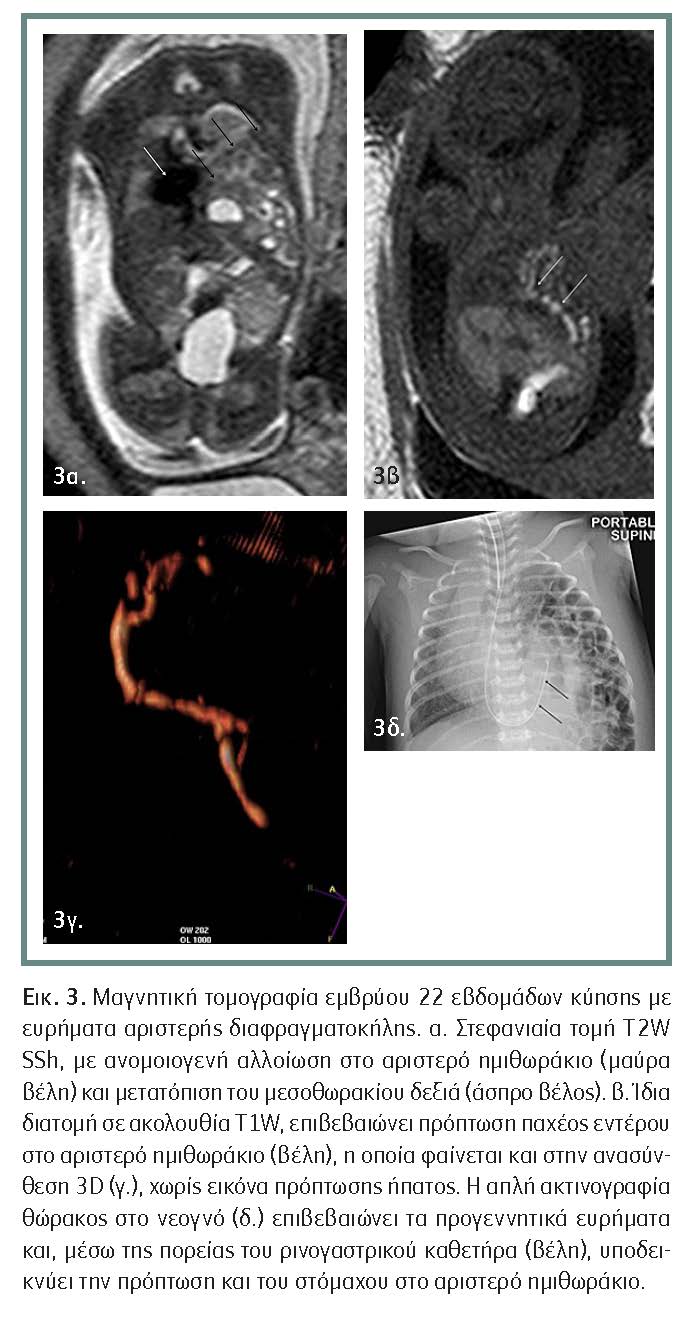
Διεπιστημονική συνεργασία
Από τα παραπάνω συμπεραίνεται πως, παρότι υπάρχει σημαντική πρόοδος στην πρώιμη διάγνωση και την έγκαιρη αντιμετώπιση των χειρουργικών συγγενών ανωμαλιών, πρέπει να δίνεται η επιλογή της διακοπής της κύησης σε περιπτώσεις σημαντικών ανωμαλιών. Η αυξημένη θνητότητα και η νοσηρότητα είναι παράγοντες που επηρεάζουν τους γονείς στη λήψη τέτοιων αποφάσεων και επιπλέον έχουν σημαντική επίπτωση στη φυσιολογική εξέλιξη του νεογνού και στη μετέπειτα ανάπτυξή του.
Απαραίτητη είναι η διεπιστημονική ενημέρωση, με παρουσία του μαιευτήρα, του εμβρυομητρικού γυναικολόγου, του γενετιστή, του νεογνολόγου και φυσικά του παιδοχειρουργού. Ο μαιευτήρας είναι αυτός που βρίσκεται πιο κοντά στους γονείς και πρέπει να οργανώσει τη διερεύνηση και την αντιμετώπιση του περιστατικού μέχρι τον τοκετό. Ο ρόλος του κλινικού γενετιστή είναι απαραίτητος στις περιπτώσεις όπου είναι πιθανόν να συνυπάρχουν επιπλέον ανωμαλίες. Ο παιδοχειρουργός είναι ο καταλληλότερος να εξηγήσει το σχέδιο δράσης μετά τη γέννηση, τους διεγχειρητικούς κινδύνους και τις απώτερες μετεγχειρητικές επιπλοκές.
Για λιγότερο σοβαρές ανωμαλίες η έγκαιρη διάγνωση και η παρακολούθηση των κυήσεων υψηλού κινδύνου σε οργανωμένες μαιευτικές μονάδες με εξειδικευμένο τμήμα υπερήχων, βοηθά στη μείωση των αδιάγνωστων περιστατικών και στη σωστή προγεννητική παρακολούθησή τους.
Η γέννηση και η επέμβαση
Η γέννηση των νεογνών υψηλού κινδύνου πρέπει να γίνεται σε μεγάλα περιφερειακά μαιευτήρια με μονάδες εντατικής θεραπείας νεογνών και οργανωμένες παιδοχειρουργικές κλινικές. Η συσσωρευμένη εμπειρία του νοσηλευτικού προσωπικού και των ιατρών στην αντιμετώπιση τέτοιων περιστατικών προσδίδει την καλύτερη δυνατή πρόγνωση για το νεογνό.
Είναι αποδεδειγμένα πλέον προτιμότερο να γεννιούνται τα νεογνά στη μονάδα όπου και θα χειρουργηθούν -in utero transfer- και να υπάρχει προγραμματισμένη και άμεση χειρουργική αντιμετώπιση, παρά να γίνεται μεταφορά των νεογνών σε αυτές μετά τη γέννηση – ex-utero transfer.
Επιπλέον, υπάρχει σε πολλές περιπτώσεις στη βιβλιογραφία διαφωνία για το βέλτιστο τρόπο γέννησης, ανάλογα με το είδος της χειρουργικής πάθησης. Φαίνεται όμως πως στην πράξη προτιμάται η καισαρική τομή, τόσο για λόγους μειωμένης έκθεσης του εμβρύου σε στρες όσο και για λόγους πρακτικούς, που έχουν να κάνουν με το συγχρονισμό των διαφορετικών ειδικοτήτων.
Ο φυσιολογικός τοκετός πριν από την 40ή εβδομάδα της κύησης -που συχνά απαιτείται- εμπεριέχει τη διαδικασία πρόκλησης τοκετού με ό,τι αυτό συνεπάγεται. Ειδικότερα, υπάρχουν σημαντικά αυξημένες πιθανότητες αποτυχίας της πρόκλησης, αλλά και ανάγκης επείγουσας καισαρικής τομής σε περίπτωση εμβρυϊκής δυσχέρειας. Μια τέτοια κατάσταση είναι ιδιαίτερα στρεσογόνος για το νεογνό και το επιβαρύνει οργανικά περισσότερο, ειδικά εν όψει της επακολουθούμενης χειρουργικής επέμβασης.
Τέλος, όποιος και αν είναι ο τρόπος γέννησης -καισαρική τομή ή φυσιολογικός τοκετός- πρέπει να λαμβάνεται σοβαρά υπόψη η σημασία που έχει το βάρος γέννησης στην επιβίωση του νεογνού μετεγχειρητικά. Είναι στατιστικά σημαντικό και αποδεδειγμένο πως για το ίδιο βάρος γέννησης, νεογνά διαφορετικής ηλικίας έχουν διαφορετικά ποσοστά νοσηρότητας και θνητότητας. Πρέπει δηλαδή να επιτυγχάνεται η μέγιστη δυνατή ωριμότητα του εμβρύου και το τουλάχιστον ελάχιστα ενδεδειγμένο για τη χειρουργική επέμβαση βάρος. Αυτό πρέπει ο μαιευτήρας να το λαμβάνει σοβαρά υπόψη του στον προγραμματισμό του τοκετού και να συμβουλεύεται τον παιδοχειρουργό για το βέλτιστο βάρος γέννησης και το βαθμό ωριμότητας του νεογνού.
Bιβλιογραφία
Grandjean H, Larroque D, Levi S. The performance of routine ultrasonographic screening of pregnancies in the Eurofetus study. Am J Obstet Gynecol 1999; 181: 446-454.
EUROCAT Working Group. Appendix 7 & Appendix 8 in Report 8: Surveillance of Congenital Anomalies in Europe 1980-99. University of Ulster, 2002: 18-19.
Stoll C, Tenconi R, Clementi M, and the Euroscan Study Group. Detection of congenital anomalies by fetal ultrasonographic examination across Europe. Community Genet, 2001; 4: 225-232.
Saari-Kemppainen A, Karjalainen O, Ostalo P, Heinonen OP. Ultrasound screening and perinatal mortality: controlled trial ofsystemic one-stage screening in pregnancy. Lancet 990; 336: 387-391.
Grandjean H, Larroque D, Levi S, and the Eurofetus Study Group. The performance of routine ultrasonographic screening of pregnancies in the Eurofetus Study. Am J Obstet Gynecol 1999; 181: 446-454.
Brook J. Hill, Bonnie N. Joe, Aliya Qayyum. Supplemental Value of MRI in Fetal Abdominal Disease Detected on Prenatal Sonography: Preliminary Experience. AJR 2005; 184: 993-998.
Garne E, Loane M, Dolk H. Prenatal diagnosis of severe structural congenital malformations in Europe. Ultrasound Obstet Gynecol 2005; 25: 6-11.
Barisic Ι, Clementi M, Hausler M. Evaluation of prenatal ultrasound diagnosis of fetal abdominal wall defects by 19 European registries. Ultrasound Obstet Gynecol 2001; 18: 309-316.
Crombleholme TM, D?Altona M, Cendrona M. Prenatal diagnosis and the pediatric surgeon: The impact of prenatal consultation on perinatal management. Journal of Pediatric Surgery, 1996; 31 (1): 156-163.
Zamora M, Gonzales N. Spontaneous resolution of a sonographically complicated fetal ovarian cyst. J Ultrasound Med 1992; 11: 567-569.
Nussbaum AR, Sanders RC, Hartman DS. Neonatal ovarian cysts: Sonographic and pathologic correlation. Radiology 1988; 168: 817-821.
Meizner I, Levy A. Fetal ovarian cysts: Prenatal ultrasonographic detection and postnatal evaluation and treatment. Am J Obstet Gynecol 1991; 164: 874-878.
Sweed Y, Puri P. Congenital diaphragmatic hernia: influence of associated malformations on survival. Arch Dis Child 1994; 69: 68-70.
Steinhorn RH, Kriesmer PJ, Green TP, et al. Congenital diaphragmatic hernia in Minnesota. Arch Pediafr Adolesc Med 1994; 148: 626-663.
Stevens TP, van Wijngaarden E, Ackerman KG. Timing of Delivery and Survival Rates for Infants With Prenatal Diagnoses of Congenital Diaphragmatic Hernia. Pediatrics, 2009; 123(2): 494-502.
Charlotte L, Huddy J, Boyd P, et al. Congenital diaphragmatic hernia: prenatal diagnosis, outcome and continuing morbidity in survivors. British Journal of Obstetrics and Gynaecology, 1999; 106: 1.192-1.196.
Phelps S, Fisher R, Partington A, et al. Prenatal ultrasound diagnosis of gastrointestinal malformations. J Pediatr Surg, 1997; 32: 438-440.
Romero R, Ghidini A, Costigan K. Prenatal Diagnosis: Does it make any difference? Obstet Gynecol, 1988: 71 (5): 739-741.
Kumaran N, Shankar KR, Lloyd DA, et al. Trends in the management and outcome of jejuno-ileal atresia. Eur J. Pediatr Surg 2002; 12: 163-167.
Barisic I, Clementi M, Hausler M, et al. Evaluation of prenatal ultrasound diagnosis of fetal abdominal wall defects by 19 European registries. Ultrasound Obstet Gynecol 2001; 18: 309-316.
Brantberg A, Blaas HG, Haugen SE, Eik-Nes SH. Characteristics and outcome of 90 cases of fetal omphalocele. Ultrasound Obstet Gynecol 2005; 26: 527-537.
Lakasing L, Cicero S, Davenport M, et al. Current outcome of antenatally diagnosed exomphalos: an 11 year review. J Pediatr Surg 2006; 41: 1.403-1.406.
Cohen-Overbeek TE, Tong WH, Hatzmann TR. Omphalocele: comparison of outcome following prenatal or postnatal diagnosis. Ultrasound Obstet Gynecol 2010; 36: 687-692.
Kominarek MA, Noelia ZS, Pierce M, Zollinger T. Perinatal Outcome in the Liveborn Infant with Prenatally Diagnosed Omphalocele. Am J Perinatol. 2011; 28 (8): 627-634.
Erguna O, Barksdalea E, Ergund FS. The timing of delivery of infants with gastroschisis influences outcome. Journal of Pediatric Surgery, 2005; 40 (2)2: 424-428.
Soares H, Silva A, Rocha G. Gastroschisi: Preterm or Term Delivery? Clinics 2010; 65 (2): 139-142.
Santiago-Munoz PC, McIntire DD, Barber RG. Outcomes of Pregnancies With Fetal Gastroschisis. Obstetrics & Gynecology 2007; 110 (3): 663-668.
Gupta DK, Sharma S, Gupta M. Outcome of Antenatally Referred Congenital Surgical Anomalies – A Pediatric Surgeon?s Perspective. Journal of Pediatric Surgical Specialties, 2015; 9(2): 1-52.
Garne E, Loane M, Dolk H. Gastrointestinal malformations: impact of prenatal diagnosis on gestational age at birth. Paediatric and Perinatal Epidemiology 2007; 21: 370-375.
Μάϊος 2016