Θεραπεία μεταστατικού καρκίνου μαστού
Ένας σημαντικός αριθμός ασθενών με πρώιμο καρκίνο μαστού θα υποτροπιάσει παρά την αρχική θεραπεία και η νόσος θα γενικευθεί. Επίσης το 10% των ασθενών εμφανίζεται εξαρχής με γενικευμένο καρκίνο.
Γράφουν οι
Πάρις Α. Κοσμίδης
Χαρ. Μπακογιάννης
Γ. Λύπας
Παθολόγοι – Ογκολόγοι
Β΄ Παθολογική – Ογκολογική Κλινική ΥΓΕΙΑ
Σύμφωνα με τα τελευταία επιδημιολογικά δεδομένα, το 20% των γυναικών με μεταστατικό καρκίνο μαστού θα επιβιώσει άνω των 5 ετών, ενώ γενικότερα η μέση επιβίωση είναι 2-3 χρόνια.
Υπάρχουν σοβαρές ενδείξεις ότι διαχρονικά οι γυναίκες με τον καρκίνο αυτό ζουν περισσότερο χρόνο χάρη στα νέα φάρμακα που χρησιμοποιούνται και στην καλύτερη γνώση των μοριακών χαρακτηριστικών των καρκινικών κυττάρων. Στόχος της θεραπείας είναι αφενός η επιμήκυνση της ζωής, αφετέρου η βελτίωση της ποιότητάς της.
Η θεραπεία σήμερα βασίζεται σε ορισμένους παράγοντες που σχετίζονται με τη βιολογία του όγκου, την έκταση του όγκου, την προσβολή ή μη σπλάχνων, την απόκριση σε προηγούμενες θεραπείες που ελήφθησαν στην αρχική φάση του καρκίνου, τις πιθανές συννοσηρότητες της ασθενούς και τις δυνατότητες για εφαρμογή πολυδιάστατης ογκολογικής αντιμετώπισης. Οι λεπτομέρειες της στρατηγικής εμφανίζονται στον πίνακα 1.
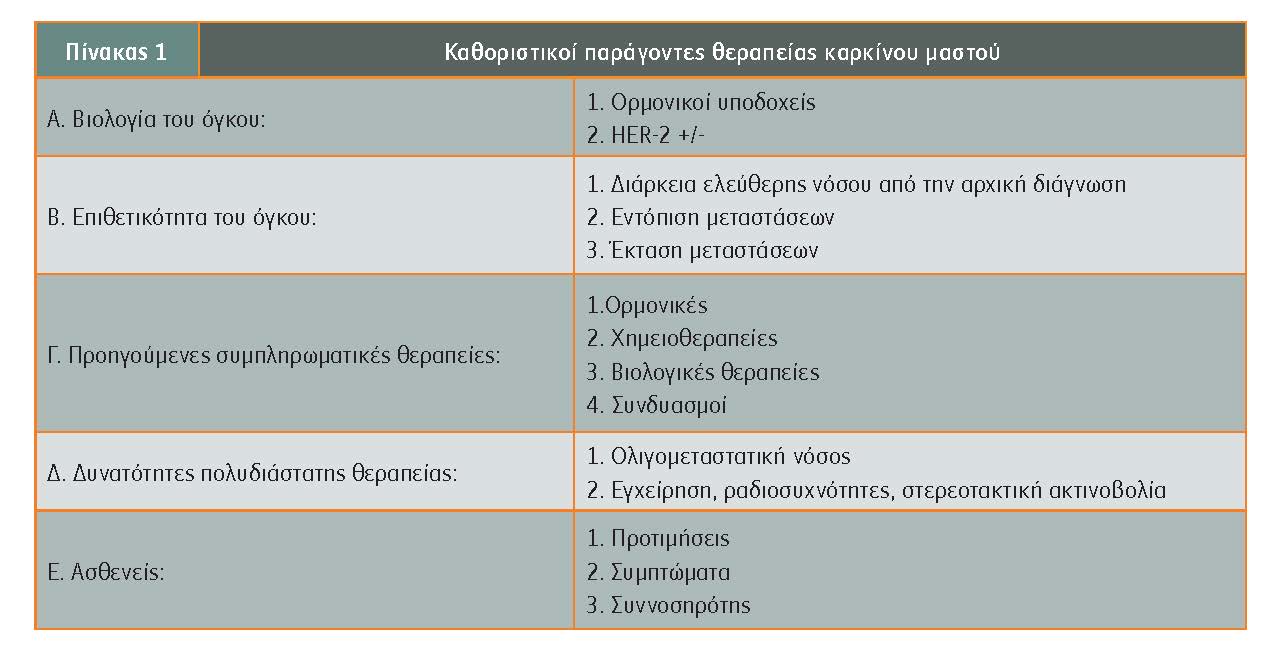
Η βιολογία του κάθε καρκίνου είναι η βάση για τη σωστή εξατομικευμένη θεραπευτική απόφαση. Η βιολογία του όγκου μεταβάλλεται με την εξέλιξη της νόσου και κατ? επέκταση η ανάγκη για επανέλεγχο της βιολογίας του καρκινικού κυττάρου μέσω βιοψίας γίνεται επιτακτική σε διάφορες φάσης της αρρώστιας.
Με βάση τη βιολογία, οι καρκίνοι του μαστού κατατάσσονται σε υπότυπους με αντίστοιχη προσαρμογή της θεραπείας, όπως φαίνεται στον πίνακα 2.
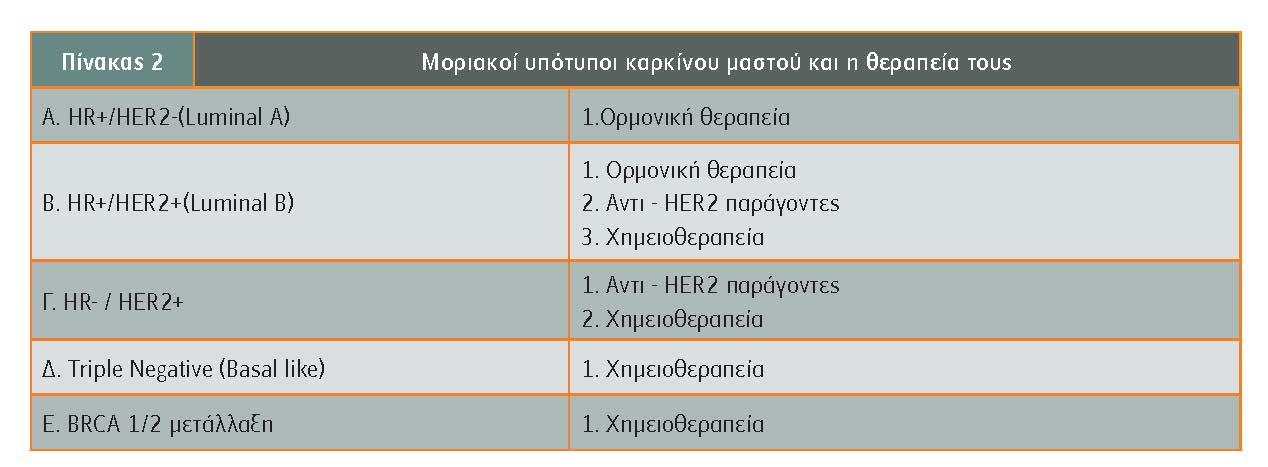
Στις περιπτώσεις των ασθενών με αρνητικούς ορμονικούς υποδοχείς ή ακόμη και σε θετικούς υποδοχείς που έχουν λάβει ορμονική θεραπεία και έχουν υποτροπιάσει, οι χημειοθεραπευτικοί και βιολογικοί παράγοντες είναι μονόδρομος, όπως φαίνεται στον πίνακα 3.

Ακολούθως θα αναφερθούν 3 κατηγορίες ασθενών με καρκίνο μαστού και θα αναλυθούν οι θεραπευτικές επιλογές. Οι 3 κατηγορίες είναι οι HER2 αρνητικές, οι HER2 θετικές και οι τριπλά αρνητικές ασθενείς.
Καρκίνος μαστού με HER2 αρνητικούς υποδοχείς
Υπάρχει μια πλειάδα χημειοθεραπευτικών φαρμάκων (όπως φαίνονται στον πίνακα 4) που στην πρώτη γραμμή έχουν αξιοσημείωτη δραστηριότητα στο μεταστατικό καρκίνο μαστού.
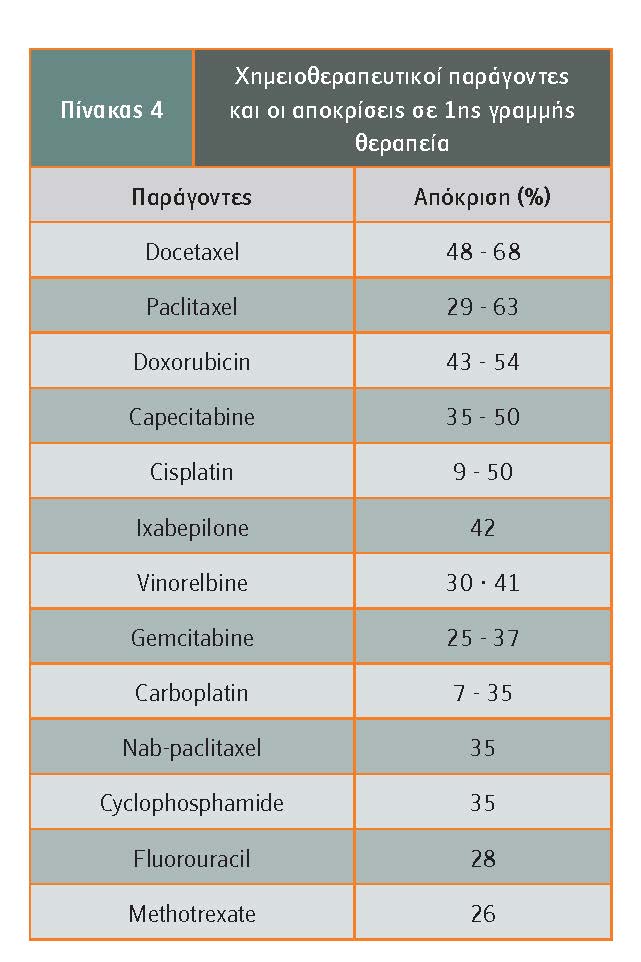
Η συνήθης τακτική στην επιλογή των φαρμάκων αυτών βασίζεται στην ταχύτητα με την οποία αναπτύσσεται ο καρκίνος και η εντόπισή του στα διάφορα όργανα. Εφόσον ο καρκίνος αναπτύσσεται βραδέως και δεν υπάρχουν σημαντικά συμπτώματα, η μονοθεραπεία είναι καλή επιλογή.
Η Capecitabine είναι συνήθως επιθυμητή επιλογή. Αντιθέτως, σε ταχύτερα αναπτυσσόμενους όγκους και κυρίως με εντοπίσεις στο ήπαρ ή τον πνεύμονα, είναι αναγκαία η επιθετικότερη αντιμετώπιση με ένα ή περισσότερα φάρμακα. Οι ταξάνες αποτελούν την αιχμή του δόρατος, με το Docetaxel ελαφρώς καλύτερο του τρισεβδομαδιαίου Paclitaxel, αν και φαίνεται ότι η χορήγηση του τελευταίου σε εβδομαδιαία βάση είναι αποτελεσματικότερη. Η συγχορήγηση Bevacizumab έχει χρησιμοποιηθεί, με αντικρουόμενα αποτελέσματα. Φαίνεται όμως ότι το διάστημα ελεύθερης νόσου επιμηκύνεται.
Οι ταξάνες είναι τοξικά φάρμακα και πολλοί ασθενείς παρουσιάζουν συμπτώματα. Το Nab-paclitaxel έχει περιορίσει τα αρνητικά συμπτώματα των ταξανών και με την καλύτερη διεισδυτικότητα στο καρκινικό κύτταρο είναι ένα υποσχόμενο νέο φάρμακο. Μπορεί να χρησιμοποιηθεί κάθε 3 εβδομάδες ή και εβδομαδιαία και υπερτερεί της Docetaxel.
Συνδυασμοί χημειοθεραπειών είναι συνήθεις στην αντιμετώπιση του μεταστατικού καρκίνου μαστού. Η Adriamycin ή η Epirubicin σε συνδυασμό με Cyclophosphamide προσφέρει ανταποκρίσεις 50%-70% και διάμεση επιβίωση 17-25 μήνες.
Ο συνδυασμός Paclitaxel και Adriamycin δίνει παρόμοια αποτελέσματα. Επίσης, το Paclitaxel μπορεί να δοθεί μετά το Docetaxel εφόσον εμφανιστεί αντοχή στο τελευταίο και αντιθέτως. Με τις ταξάνες μπορεί να συνδυαστεί το Capecitabine. Ένας κλασικός συνδυασμός είναι των Methotrexate, Cyclophosphamide και Fluorouracil.
Είναι σημαντικό να λαμβάνεται πάντα υπόψη η ηλικία και η γενική κατάσταση των ασθενών. Σε ηλικιωμένα άτομα με περιορισμένη λειτουργική ικανότητα η μονοθεραπεία είναι προτιμητέα. Φάρμακα όπως Vinorelbine, Liposomal Doxorubicin, Mitoxantrone, Gemcitabine, Eribulin βοηθούν στην αντιμετώπιση των ασθενών αυτών.
Τέλος, απαραίτητο συμπλήρωμα των ανωτέρω θεραπειών στις ασθενείς εκείνες που έχουν οστικές μεταστάσεις, είναι η προσθήκη των διφωσφονικών ή του Denosumab.
Καρκίνος μαστού με HER2 θετικούς υποδοχείς
Οι ασθενείς με προχωρημένο καρκίνο του μαστού, που είναι HER2 θετικές, μπορούν να ωφεληθούν με θεραπεία που στοχεύει τον HER2 υποδοχέα σε συνδυασμό με επιλεγμένους χημειοθεραπευτικούς παράγοντες. Η επιλογή γίνεται από τις ασθενείς που είναι είτε θετικές για HER2 με FISH είτε 3+ με ανοσοϊστοχημεία (IHC).
Η αντί-HER2 θεραπεία (π.χ. Trastuzumab, Lapatinib) σε συνδυασμό με χημειοθεραπεία, πρέπει να χορηγείται πρώιμα σε όλες τις ασθενείς με προχωρημένο καρκίνο του μαστού που είναι HER2 θετικές και δεν έχουν αντένδειξη για τέτοια θεραπεία.
Ως πρώτης γραμμής θεραπεία χορηγείται το Trastuzumab σε συνδυασμό με χημειοθεραπευτικούς παράγοντες. Τυχαιοποιημένες μελέτες έχουν δείξει όφελος από τη χορήγηση του Trastuzumab με τέτοιους παράγοντες όπως Paclitaxel με ή χωρίς Carboplatin, με Docetaxel, με Vinorelbine και με Capecitabine.
Διάφορες μελέτες έχουν δείξει όφελος από τη συνέχιση της θεραπείας με Trastuzumab σε συνδυασμό με έναν άλλο χημειοθεραπευτικό παράγοντα, έπειτα από επιδείνωση της νόσου σε θεραπεία που περιλάμβανε Trastuzumab. Εντούτοις η καλύτερη διάρκεια χορήγησης του Trastuzumab σε ασθενείς με μακροχρόνιο έλεγχο της νόσου είναι άγνωστη.
Σε ασθενείς που λαμβάνουν θεραπεία με τον συνδυασμό Trastuzumab και Doxorubicin/Cyclophosphamide, η συχνότητα σημαντικής καρδιακής δυσλειτουργίας φθάνει μέχρι 27% στη μεταστατική φάση της νόσου και είναι πολύ υψηλή για να χρησιμοποιηθεί αυτός ο συνδυασμός εκτός των ορίων μιας προοπτικής κλινικής μελέτης.
Το Pertuzumab είναι ένα ανασυνδυασμένο εξανθρωποποιημένο μονοκλωνικό αντίσωμα που αναστέλλει το διμερισμό του HER2 και τη σηματοδότησή του προς τον πυρήνα του κυττάρου.
Το Pertuzumab και το Trastuzumab συνδέονται με διαφορετικούς επιτόπους του υποδοχέα HER2 και έχουν συμπληρωματικούς μηχανισμούς δράσης. Η προσθήκη του Pertuzumab στην πρώτης γραμμής θεραπεία με Trastuzumab και Docetaxel (σε μία τυχαιοποιημένη μελέτη φάσης ΙΙΙ) έχει συνδεθεί με βελτίωση του ποσοστού των αποκρίσεων, της επιβίωσης χωρίς επιδείνωση της νόσου (PFS) και με μία τάση προς βελτίωση της συνολικής επιβίωσης. Το Pertuzumab έχει προσφάτως εγκριθεί από το FDA και αναμένεται η έγκριση από τον ΕΜΑ.
Το Ado-Trastuzumab emtansine (T-DM1) αναπτύχθηκε από τη σύζευξη αντισώματος και του κυτταροτοξικού φαρμάκου DM1 (ένας αναστολέας των μικροσωληνίσκων). Το T-DM1 έχει δείξει καλύτερη αποτελεσματικότητα όσον αφορά στο PFS και καλύτερο προφίλ όσον αφορά στην τοξικότητα, όταν συγκρίθηκε ως πρώτης γραμμής θεραπεία με τον συνδυασμό trastuzumab και docetaxel. Το T-DM1 δεν έχει εγκριθεί ακόμη από τον ΕΜΑ ή το FDA.
Η θεραπεία με Lapatinib σε συνδυασμό με Capecitabine είναι μια επιλογή για ασθενείς με HER2 θετική νόσο, έπειτα από επιδείνωση σε θεραπεία που περιέχει Trastuzumab.
Σε μια μελέτη φάσης ΙΙΙ, συγκρίθηκε Lapatinib και Capecitabine έναντι μόνο Capecitabine, σε γυναίκες με προχωρημένο ή μεταστατικό καρκίνο του μαστού, ανθεκτικό στο Trastuzumab, κατά τη μεταστατική φάση της νόσου και με προηγούμενη θεραπεία με μία ανθρακυκλίνη και μία ταξάνη, είτε σε μεταστατική είτε σε συμπληρωματική φάση. Ο χρόνος μέχρι την επιδείνωση της νόσου (TTP) αυξήθηκε στην ομάδα που έλαβε τη συνδυασμένη θεραπεία όταν συγκρίθηκε με την ομάδα που έλαβε μονοθεραπεία με Capecitabine (8,4μήνες έναντι 4,4 μήνες, HR 0,49 95% CI, 0,34 – 0,71, P<0,001).
Ο συνδυασμός Trastuzumab και Lapatinib φαίνεται να υπερέχει όσον αφορά στη συνολική επιβίωση έναντι της μονοθεραπείας με Lapatinib, σε ασθενείς που επιδεινώνονται έπειτα από ή υπό θεραπεία με ανθρακυκλίνη, ταξάνη ή trastuzumab (δεν έχει εγκριθεί από τον ΕΜΑ ή το FDA).
Καρκίνος μαστού τριπλά αρνητικός
Τριπλά αρνητικός καρκίνος του μαστού (TNBC) είναι ο ιστολογικός υπότυπος που χαρακτηρίζεται από απουσία έκφρασης υποδοχέων οιστρογόνων, προγεστερόνης και HER-2. Οι TNBC υποτροπιάζουν πιο συχνά σε σύγκριση με τους ορμονοεξαρτώμενους τύπους, τόσο τοπικοπεριοχικά όσο και με μεταστατικές εστίες στους πνεύμονες και στον εγκέφαλο, αλλά όχι στα οστά. Η διάμεση επιβίωση στην περίπτωση εντοπίσεως στο ΚΝΣ είναι χαμηλότερη του εξαμήνου. Οι περισσότερες υποτροπές σε εξαιρεθέντα νεοπλάσματα αυτής της κατηγορίας συμβαίνουν εντός τριετίας. Μετά την τριετία η συχνότητα των υποτροπών μειώνεται σημαντικά.
Χημειοθεραπεία στον TNBC
Ο βασικός άξονας της συστηματικής θεραπείας του TNBC είναι η κυτταροτοξική χημειοθεραπεία, καθώς οι ορμονικές και οι αντι-HER2 θεραπείες δεν είναι αποτελεσματικές. Οι χημειοθεραπευτικοί παράγοντες μπορούν να χορηγηθούν είτε ως μονοθεραπεία είτε σε συνδυασμούς (βλ. πίνακα 5).
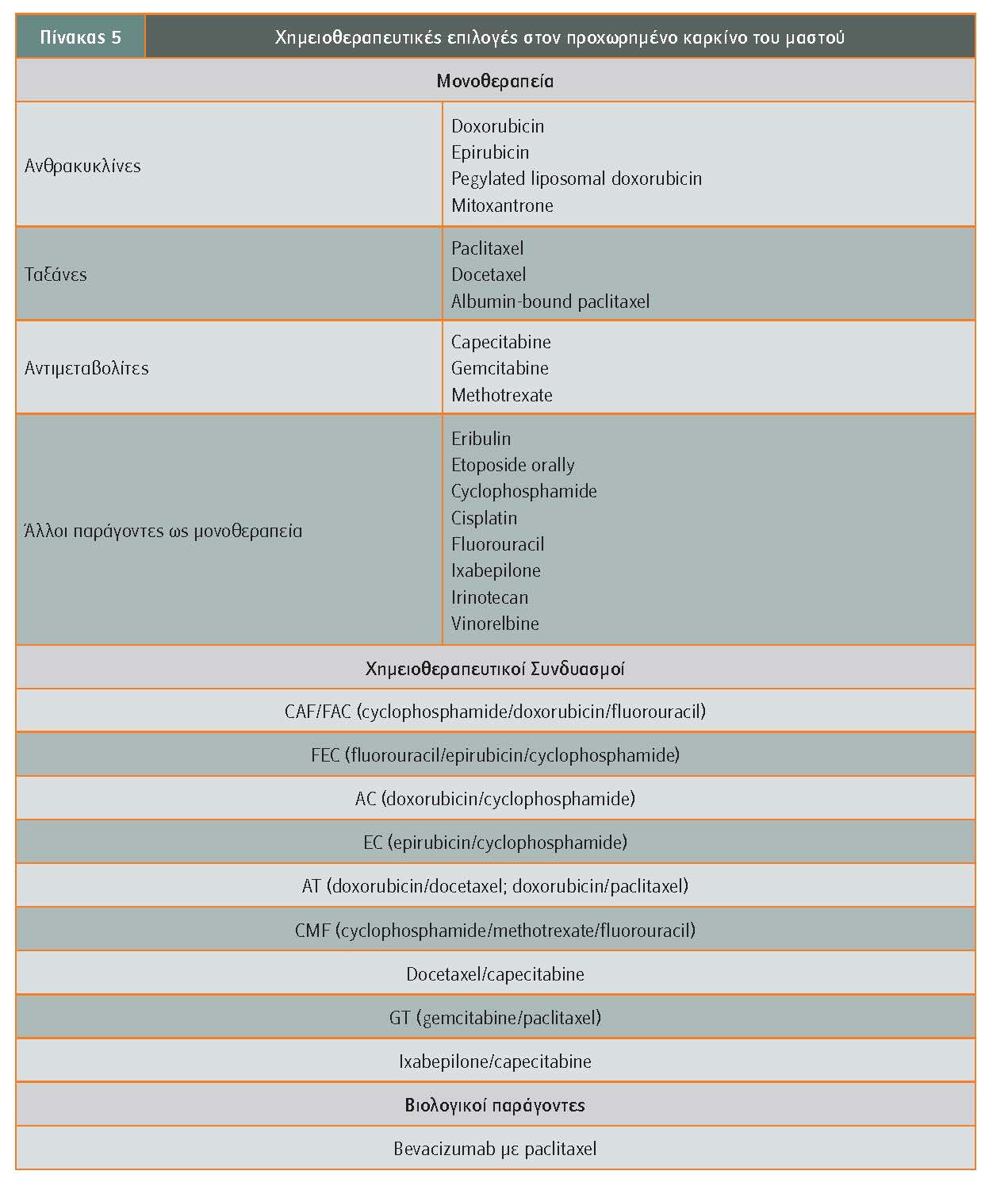
Οι χημειοθεραπευτικοί συνδυασμοί επιτυγχάνουν συχνότερες και μεγαλύτερης έκτασης και διάρκειας ανταποκρίσεις, καθυστερώντας την εξέλιξη της νόσου, σε σύγκριση με τη μονοθεραπεία. Εντούτοις, είναι πιο τοξικοί και έχουν μικρό όφελος στη συνολική επιβίωση. Επιπλέον, με τις μονοθεραπείες δεν χρειάζονται τόσο συχνά μειώσεις δόσεων.
Όταν μια ασθενής διαγνωστεί με υποτροπή καρκίνου του μαστού ή μεταστατική νόσο, η 1ης γραμμής θεραπεία συνεχίζεται συνήθως μέχρι την πρόοδο της νόσου ή μέχρι η τοξικότητα ή η επιδείνωση της ποιότητας ζωής της να το επιβάλει. Σημειώνεται ότι δεν υπάρχουν δεδομένα που να τεκμηριώνουν όφελος στην επιβίωση με την παρατατεταμένη χημειοθεραπεία και πάντοτε πρέπει να σταθμίζεται η απόκριση της νόσου σε σχέση με την ποιότητα ζωής.
Κληρονομούμενος TNBC (Γαμετική μετάλλαξη BRCA1/2)
Το σύνδρομο κληρονομικού καρκίνου μαστού και ωοθηκών οφείλεται σε γαμετική μετάλλαξη (germline mutation) των γονιδίων BRCA1& 2. Στην πλειονότητα (>80%) των ασθενών που εμφανίζουν καρκίνο του μαστού, στο πλαίσιο γαμετικής μετάλλαξης του BRCA1, ο ιστολογικός τύπος είναι τριπλά αρνητικός, όπως επίσης στο 20% των ασθενών με μετάλλαξη του BRCA2.
Με βάση το ότι σχεδόν οι μισές από τις γυναίκες αυτές δεν έχουν σχετικό οικογενειακό ιστορικό, οι κατευθυντήριες οδηγίες του National Comprehensive Cancer Network συνιστούν όλες οι γυναίκες που διαγιγνώσκονται με TNBC πριν από την ηλικία των 60 να υποβάλλονται σε γονιδιακό έλεγχο των BRCA1 και 2, ανεξαρτήτως υπάρξεως ή όχι οικογενειακού ιστορικού, καθώς οι πιθανότητες να φέρουν παθογόνο μετάλλαξη ανέρχονται σε τουλάχιστον 10%.
Σε ασθενείς με μεταστατικό καρκίνο του μαστού πρέπει, όταν είναι εφικτό, να λαμβάνεται βιοψία επιβεβαίωσης της ύποπτης εστίας, με σκοπό την επανεπιβεβαίωση των ER, PR και HER2, καθώς περιγράφονται ποσοστά αποκλίσεων μεταξύ πρωτοπαθούς και μεταστατικής εστίας, μεταξύ 5% και 28%.
Μετάλλαξη του γονιδίου BRCA1
Εξαιτίας του ρόλου του BRCΑ1 στην επιδιόρθωση βλαβών του DNA και στον έλεγχο του κυτταρικού κύκλου, θεωρήθηκε ότι τα νεοπλάσματα που αναπτύσσονται σε έδαφος μεταλλαγμένου BRCA1 θα είναι ευαίσθητα σε διάφορους παράγοντες βλάβης του DNA, όπως τα άλατα της πλατίνας (καρβοπλατίνη ή σισπλατίνη). Κλινικές μελέτες έδειξαν σημαντικά ποσοστά αποκρίσεως, όμως περιλάμβαναν λίγους ασθενείς και δεν ανακοίνωσαν ποσοστά επιβίωσης αυτών των ασθενών. Πιο υποσχόμενα είναι τα δεδομένα για μια οικογένεια παραγόντων, που λέγονται αναστολείς-PARP και οι οποίοι βρίσκονται σε στάδιο κλινικών μελετών.
Σποραδικός TNBC
Αν και υπάρχουν μοριακές ομοιότητες μεταξύ των σποραδικών TNBC και αυτών που σχετίζονται με το BRCA1, δεν υπάρχουν δεδομένα από κλινικές μελέτες που να τεκμηριώνουν ότι είναι πιο ευαίσθητοι σε πλατινούχους παράγοντες απ? ό,τι άλλοι ιστολογικοί υπότυποι. Έχουν διεξαχθεί αρκετές σχετικές μελέτες συνδυασμών, χωρίς να τεκμηριώνουν όφελος στην επιβίωση, σε σύγκριση με τις συνήθεις θεραπείες.
Bιβλιογραφία
1. NCCN Guidelines Version 2, 2013.
2. Cardoso F, Harbeck N, Fallowfield L, et al. Locally recurrent or metastatic breast cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 23 2012: (Suppl 7); vii11 – vii19.
3. Seidman A, Berry DA, Cirrincione C, et al. Randomized phase III trial of weekly compared with every 3weeks Paclitaxel for metastatic breast cancer with Trastuzumab for all HER2 overexpressions and random assignment to trastuzumab or not in HER2 nonoverxpressions: final results of Cancer and Leukemia Group B protocol 9840. J Clin Oncol 2008; 26: 1.642 – 1.649.
4. Burstein HJ, Keshaviah A, Baron AD, et al. Trastuzumab plus Vinorelbine or Taxane chemotherapy for HER2 overexpressing metastatic breast cancer: the Trastuzumab and Vinorelbine or Taxate study. Cancer 2007; 110: 965 – 972.
5. Robert N, Leyland-Jones B, Asmar L, et al. Randomized phase III study of Trastuzumab, Paclitaxel and Carboplatin compared with Trastuzumab and Paclitaxel in women with HER2 overexpressing metastatic breast cancer. J Clin Oncol 2006; 24: 2.786 – 2.792.
6. Yamamoto D, Iwase S, Kitamura K, et al. A phase II study of Trastuzumab and Capecitabine for patients with HER2 overxpressing metastatic breast cancer: Japan Breast Cancer Research Network (JBCRN)00 Trial. Cancer Chemother Pharmacol 2008; 61: 509 – 514.
7. Bartsch R, Wenzel C, Altorjai G, et al. Capecitabine and Trastuzumab in heavily pretreated metastatic breast cancer. J Clin Oncol 2007, 25: 3.853 – 3.858.
8. Von Minckwitz G, Zielinski C, Maarteense E, et al. Capecitabine vs Capecitabine + Trasuzumab in patients with HER2 positive metastatic breast cancer progressing during Trastuzumab treatment: The TBP phase II study. J Clin Oncol 2008, 26 (Suppl 15): Abstract 1.025.
9. Seidman A, Hudis C, Pierri MK, et al. Cardiac dysfunction in the Trastuzumab clinical trials experience. J Clin Oncol 2002; 20: 1.215 – 1.221.
10. Baselga J, Cortes J, Kim SB, et al. Pertuzumab plus Trastuzumab plus Docetaxel for metastatic breast cancer. N Engl J Med 2012; 366: 109 – 119.
11. Hurvitz SA, Dirix L, Kocsis J, et al. Phase II randomized study of Trastuzumab emtansine versus Trastuzumab plus Docetaxel in patients with human epidermal growth factor receptor2 positive metastatic breast cancer. J Clin Oncol 2013, 31: 1.157 – 1.163.
12. Geyer C, Forster J, Lindquist D, et al. Lapatinib plus Capecitabine for HER2 positive advanced breast cancer. N Engl J Med 2006; 355: 2.733 – 2.743.
13. Lin NU, Vanderplas A, Hughes ME, et al. Clinicopathologic features, patterns of recurrence, and survival among women with triple-negative breast cancer in the National Comprehensive Cancer Network. Cancer 2012; 118: 5.463.
14. Turner N, Tutt A, Ashworth A. Hallmarks of CBRCAnessE in sporadic cancers. Nat Rev Cancer 2004; 4: 814.
15. Smid M, Wang Y, Zhang Y, et al. Subtypes of breast cancer show preferential site of relapse. Cancer Res 2008; 68: 3.108.
16. Lin NU, Claus E, Sohl J, et al. Sites of distant recurrence and clinical outcomes in patients with metastatic triple-negative breast cancer: high incidence of central nervous system metastases. Cancer 2008; 113: 2.638.
17. Amir E, Clemons M, Freedman OC, et al. Tissue confirmation of disease recurrence in patients with breast cancer: Pooled analysis of two large prospective studies (abstract #1007). J Clin Oncol 2010; 28: 15s.
18. Khasraw M, Brogi E, Seidman AD. The need to examine metastatic tissue at the time of progression of breast cancer: is re-biopsy a necessity or a luxury? Curr Oncol Rep 2011; 13: 17.
19. Baselga J, Gomez P, Awada A, et al. The addition of cetuximab to cisplatin increases overall response rate and progression-free survival ini metastatic triple negative breast cancer: results of a randomized phase II study (abstract 2740). Data presented at the 2010 meeting of the European Society of Medical Oncology, Milan, Italy, October 8-12, 2010. http://annonc.oxfordjournals.org/content/21/suppl_8 (Accessed on September 07, 2011).
20. Isakoff SJ, Goss PE, Mayer EL, et al. TBCRC009: A multicenter phase II study of cisplatin or carboplatin for metastatic triple-negative breast cancer and evaluation of p63/p73 as a biomarker of response (abstract). J Clin Oncol 2011; 29: 86s. Abstract available online at http://www.asco.org/ASCOv2/Meetings/Abstracts?&vmview=abst_detail_view&confID=102&abstractID=76639 (Accessed on July 08, 2011).
21. www.nccn.org (last accessed 20 May 2013).
Οκτώβριος 2016








































