Προγραμματισμένη επείγουσα περιγεννητική χειρουργική αντιμετώπιση
Στη μέχρι τώρα πορεία μου στην ιατρική δεν συνάντησα κάποιον που να μην προτιμούσε να αντιμετωπίσει έναν προγραμματισμένο διαγνωσμένο ασθενή από ένα επείγον και απρόβλεπτο περιστατικό.
Γράφει ο
Στέλιος Υψηλάντης
Παιδοχειρουργός
Παίδων ΜΗΤΕΡΑ
Κάθε ειδικός θα ήθελε να ξέρει τον τόπο και τον χρόνο όπου θα αντιμετωπίσει ένα απρόοπτο ιατρικό συμβάν. Ο καρδιολόγος θα ήθελε να ξέρει πότε ο ασθενής του θα κάνει ισχαιμικό επεισόδιο, όπως ο χειρουργός τη διάτρηση στομάχου και ο παιδίατρος την οξεία αναπνευστική δυσχέρεια. Η εξέλιξη της προγεννητικής διάγνωσης τα τελευταία χρόνια ήταν εκρηκτική. Την ώθηση έδωσε η διαπίστωση των νεογνολόγων, των παιδοχειρουργών και των μαιευτήρων ότι αντιμετώπιζαν παθήσεις μετά τη γέννηση, τις οποίες όμως θα ήταν καλό να γνώριζαν από πριν.
Όταν κάτι το γνωρίζεις καλά, το απομυθοποιείς. Όλη αυτή η εξέλιξη οδήγησε στην απομυθοποίηση του εμβρύου και μόνο τότε μπορέσαμε να αντιληφθούμε το έμβρυο ως ασθενή. Από το homunculus των Ρωμαίων και τον σπόρο του Δαρβίνου καταφέραμε να γνωρίζουμε, με την ανάπτυξη της μοριακής βιολογίας και του προγεννητικού ελέγχου, τα βασικά βήματα όλης της ενδομήτριας περιόδου, από τη στιγμή της γονιμοποίησης μέχρι τη γέννηση, κατανοώντας την οργανογένεση. Αποτέλεσμα ήταν η έγκαιρη διάγνωση των συγγενών ανωμαλιών και επιτακτική η χάραξη προγεννητικής και περιγεννητικής στρατηγικής για την αντιμετώπισή τους.
Διαγνωστικά μέσα
Σύμφωνα με τη διεθνή βιβλιογραφία, το 3% των γεννημένων ζώντων νεογνών παρουσιάζει συγγενείς ανωμαλίες και το 1% θα απεβίωνε χωρίς χειρουργική παρέμβαση. Με δεδομένο ότι η ολοκλήρωση της οργανογένεσης έχει συντελεστεί μέχρι το τέλος της 12ης εβδομάδας της κύησης, η εντόπιση των συγγενών ανωμαλιών αναμένεται, σύμφωνα με νεότερες έρευνες, ήδη από τη 14η εβδομάδα, αλλά αυτές τεκμηριώνονται μόνο μετά τη 18η – 20ή εβδομάδα της κύησης. Σε αυτό βοήθησαν σημαντικά η ευρεία χρήση και η εκμετάλλευση των δυνατοτήτων του προγεννητικού υπερηχογραφήματος. Τα ποσοστά ακρίβειας του προγεννητικού υπερηχογραφήματος είναι εντυπωσιακά για τα περισσότερα συστήματα. Έτσι, για το κεντρικό νευρικό σύστημα είναι 96% – 100%, για το ερειστικό 80% – 94%, για το γαστρεντερικό 60% – 92% και για το ουροποιογεννητικό 50% – 100%. Βέβαια, το προγεννητικό υπερηχογράφημα είναι μία δυναμική εξέταση η οποία είναι άρρηκτα συνδεδεμένη με την ικανότητα του ιατρού που την εκτελεί να αναγνωρίζει, ή να πιθανολογεί, ή να αποκλείει τις συγγενείς ανωμαλίες. Έτσι, ο παιδοχειρουργός συνεκτιμώντας την κλινική εικόνα βγαίνει από διαγνωστικά αδιέξοδα. Βασικά όπλα στην προγεννητική διάγνωση είναι, εκτός από το υπερηχογράφημα, η αμνιοκέντηση, η λήψη χορειακών λαχνών, η μαγνητική τομογραφία καθώς και οι βιοχημικές, ενζυματικές και γενετικές αναλύσεις με διαδερμική λήψη αίματος από την ομφαλική φλέβα και των εμβρυϊκών κυττάρων της κυκλοφορίας της μητέρας.
Η μαγνητική τομογραφία είναι μία ασφαλής διαγνωστική μέθοδος για το 2ο – 3ο τρίμηνο της κύησης, χωρίς γνωστούς κινδύνους για το έμβρυο. Κατά καιρούς τέθηκαν ερωτήματα όσον αφορά στην αύξηση της θερμοκρασίας των εμβρυϊκών δομών από τη μαγνητική ακτινοβολία και στην πρόκληση ακουστικών βλαβών στο έμβρυο, χωρίς όμως αυτές να τεκμηριωθούν από κλινικά ή πειραματικά αποτελέσματα. Παρ? όλα αυτά, είναι καλύτερα να αποφεύγεται κατά το 1ο τρίμηνο και να γίνεται μόνο για διαγνωστικούς λόγους της μητέρας. Η αμνιοκέντηση είναι μία διαγνωστική μέθοδος χαμηλού κινδύνου, που γίνεται κατά τη 15η – 16η εβδομάδα και δίνει πληροφορίες οι οποίες έχουν σχέση με χρωμοσωμικές ανωμαλίες, βιοχημικές και ενζυματικές αναλύσεις και με τη δημιουργία καρυότυπου. Η λήψη χορειακών λαχνών μπορεί να γίνει λίγο νωρίτερα (10η – 14η εβδομάδα) για να ταυτοποιηθεί ο καρυότυπος και να γίνει ενζυματική και γενετική μελέτη.
Καθορισμός περιγεννητικής στρατηγικής
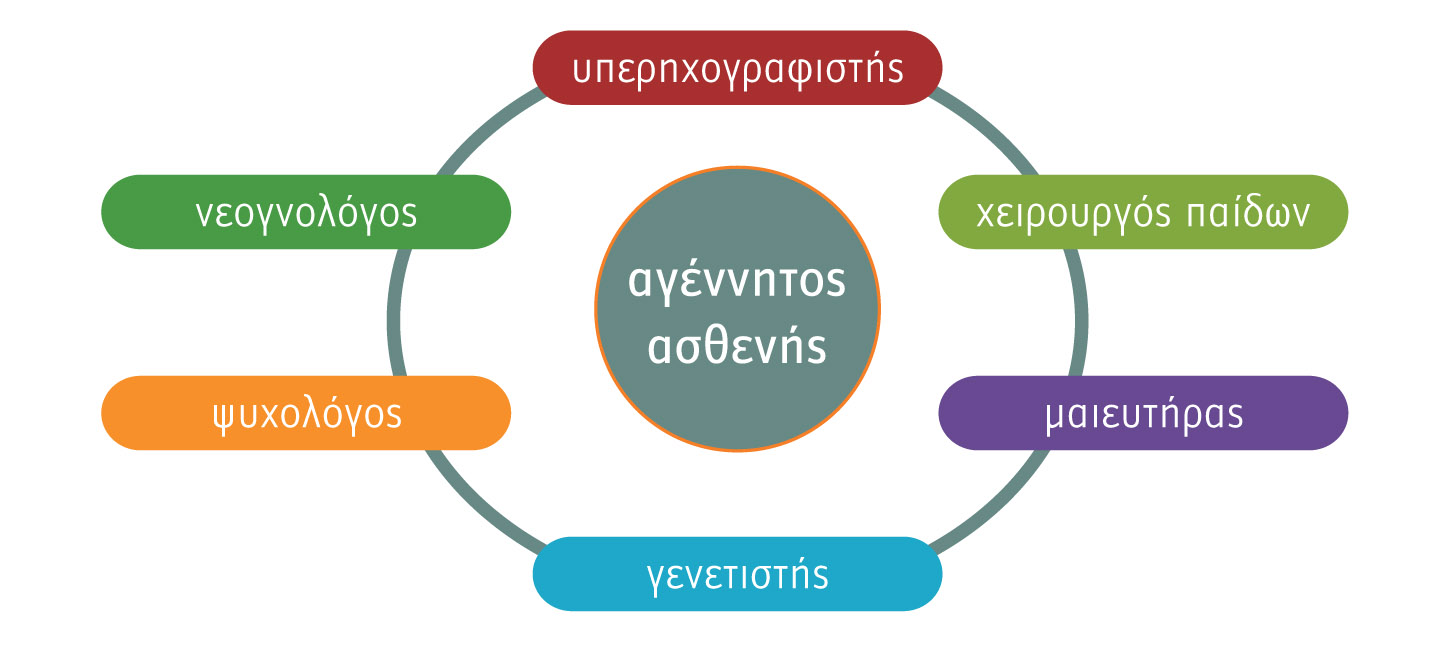
Η αιτιολογία των συγγενών ανωμαλιών συνάγεται μόνο από στατιστικά δεδομένα. Έχουν ενοχοποιηθεί κατά 20% οι γενετικοί και κατά 10% οι περιβαλλοντικοί παράγοντες, ενώ σε ποσοστό 70% η αιτιολογία είναι άγνωστη. Είναι εύλογο ότι οφείλουμε να βρούμε τον τρόπο ώστε να τις αντιμετωπίσουμε ανεξάρτητα από αδιευκρίνιστες αιτιολογίες. Βασικός παράγων για να χαραχθεί μία ενιαία στρατηγική στην αντιμετώπιση των χειρουργικών συγγενών ανωμαλιών είναι η ύπαρξη συμβουλευτικής επιστημονικής ομάδας (ΣΕΟ) (εικόνα 1), που θα αποτελείται από τον θεράποντα μαιευτήρα, τον υπερηχογραφιστή, έναν ψυχολόγο, έναν γενετιστή, έναν νεογνολόγο και έναν παιδοχειρουργό, καθώς και, κατά περίπτωση, έναν χειρουργό άλλης ειδικότητας εάν η ανωμαλία αφορά σε αντίστοιχο σύστημα. Τα κύρια ερωτήματα που θα πρέπει να απαντηθούν είναι, πρώτον, η συνέχιση ή όχι της κύησης και, δεύτερον, ο προγραμματισμός του τόπου, του χρόνου και του τρόπου του τοκετού. Όταν εντοπιστεί μία συγγενής ανωμαλία στο έμβρυο, η ΣΕΟ πρέπει να το αντιμετωπίσει ως ασθενές. Ο ρόλος του υπερηχολόγου και του γενετιστή είναι η σαφής διάγνωση μετά την «εξέταση» του εμβρύου, ο νεογνολόγος και ο παιδοχειρουργός συντονίζουν μαζί με τον μαιευτήρα την εξέλιξη και τις παρεμβάσεις στην εγκυμοσύνη και ο ψυχολόγος υποστηρίζει τους γονείς, ώστε να αντιμετωπίσουν όσον το δυνατόν καλύτερα την κατάσταση. Έχει διαπιστωθεί ότι πολλά ζευγάρια χωρίζουν (διπλάσιο ποσοστό σε σχέση με τον υπόλοιπο πληθυσμό) έπειτα από εγκυμοσύνη νεογνού με συγγενή ανωμαλία, γιατί υποσυνείδητα θεωρούν ότι η σχέση τους οδήγησε σε αυτό το αποτέλεσμα. Πρέπει να δοθούν απαντήσεις, από όλη την ομάδα, εάν τέτοια προβλήματα θα εμφανίσουν και άλλες εγκυμοσύνες ή εάν υπάρχει τρόπος αυτό να είναι γνωστό σε αρχικά στάδια της κύησης.
Επίσης, αυτές οι οικογένειες πρέπει να υποστηριχτούν για μια χαμένη εγκυμοσύνη ή για το γεγονός ότι θα βρεθούν μπροστά σε νέες χειρουργικές επεμβάσεις. Προσοχή πρέπει να δοθεί και στον εντοπισμό ή στην πιθανότητα ύπαρξης συνυπαρχουσών ανωμαλιών και να διευκρινιστεί αν η ανωμαλία είναι μονήρης ή είναι μέρος ενός συνδρόμου. Εάν το έμβρυο έχει μία ανωμαλία το ποσοστό χρωμοσωμικών ανωμαλιών είναι 10%, ενώ στα έμβρυα με δύο ή περισσότερες ανωμαλίες είναι 30%. Σε ένα λεπτομερές ιστορικό πρέπει να διευκρινίζονται η πιθανότητα λήψης φαρμακευτικών ουσιών, μεταβολικές διαταραχές της μητέρας, επιπλοκές της εγκυμοσύνης, προηγούμενες εγκυμοσύνες και η έκβασή τους, καθώς και κάθε οικογενειακό ιστορικό συγγενών ανωμαλιών και γενετικών δυσλειτουργιών, εμβαθύνοντας το κάθε μέλος της ΣΕΟ στον δικό του τομέα. Όπως, για παράδειγμα, στην τρισωμία 21 θα πρέπει να διερευνηθεί η πιθανότητα ατρησίας δωδεκαδακτύλου και το αντίθετο, ή ο εντοπισμός ενός κυστικού υγρώματος (εικόνα 2) θα θέσει την υποψία μονοσωμίας Χ. Ορισμένες δομικές ανωμαλίες, όπως η γαστρόσχιση, οφείλονται σε αγγειακές βλάβες και παράγοντες που θα μπορούσαν να τις προκαλέσουν είναι το κάπνισμα και η νεαρή ηλικία της μητέρας. Σε αντίθεση, ο εξόμφαλος είναι συνδυασμένος με ανευπλοϊδία σε ποσοστό 40% και μέρος του συνδρόμου Beckwith-Wiedemann σε ποσοστό 22%. Συγκεντρώνοντας όλες τις πληροφορίες θα πρέπει να αποφασιστεί ποια άλλη διαγνωστική μέθοδος χρειάζεται ώστε να ταυτοποιηθεί πλήρως η ανωμαλία και να καθοδηγηθούν οι θεράποντες και οι γονείς που έχουν να αντιμετωπίσουν το πρόβλημα.
Τρόπος – χρόνος – τόπος
Μέχρι πρόσφατα, το βασικό ερώτημα σε μια κύηση με συγγενή χειρουργική ανωμαλία ήταν η συνέχιση ή η διακοπή της. Όμως, σήμερα τίθεται και το ερώτημα του τρόπου, του χρόνου και του τόπου που θα πραγματοποιηθεί ο τοκετός. Είναι βασικό ότι οι αιτίες διακοπής της εγκυμοσύνης είναι σαφώς καθορισμένες από ιατρική άποψη (πίνακας 1).

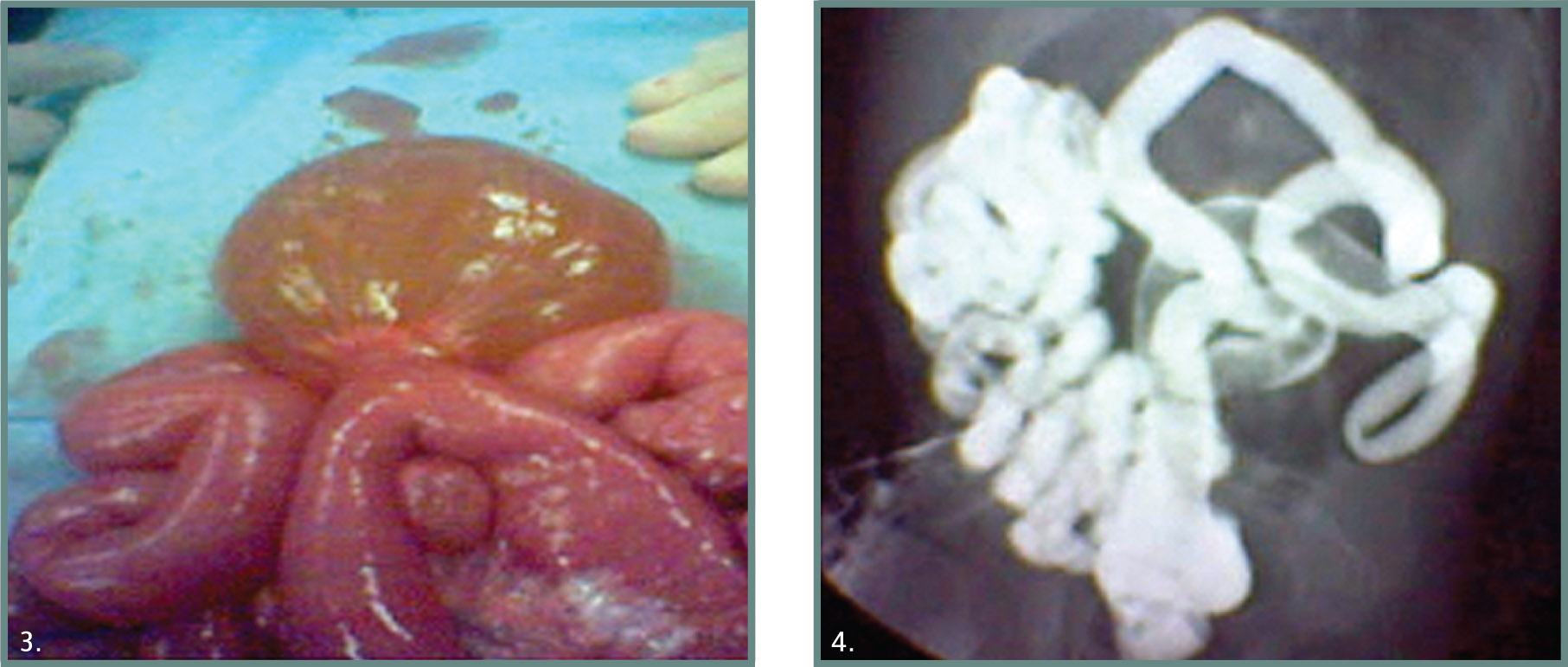
Στους πίνακες 2, 3, 4 καθορίζονται ο τρόπος, ο χρόνος και ο τόπος του τοκετού. Σε ορισμένες ανωμαλίες ενδείκνυται ο τοκετός με καισαρική τομή, είτε λόγω της δυστοκίας που προκαλεί η πάθηση είτε γιατί το πάσχον νεογέννητο ωφελείται από μια άμεση χειρουργική αντιμετώπιση, όπως σε έναν ραγέντα εξόμφαλο ή σε μια ανοιχτή μυελομηνιγγοκήλη. Ο λόγος για πρόωρο τοκετό είναι μοναδικός για κάθε πάθηση, αλλά απαντά στο ίδιο ερώτημα: η συνέχιση της εγκυμοσύνης θα βλάψει το νεογνό; Ανωμαλίες που προκαλούν ισχαιμία πρέπει να διορθώνονται όσο το δυνατόν γρηγορότερα, όπως σε μια επικείμενη συστροφή εντέρου λόγω μορφώματος του εντέρου (εικόνα 3) ή ανωμαλίας στροφής και καθήλωσης (εικόνα 4). Στη γαστρόσχιση το τοίχωμα του εξωτερικευμένου εντέρου γίνεται παχύ και φλεγμονώδες, με αποτέλεσμα τη μειωμένη κινητοποίησή του και λειτουργικότητά του. Τα ποσοστά επιβίωσης είναι υπέρ της μεταφοράς του εμβρύου εκεί που θα γίνει η επέμβαση (επιβίωση 90,5%) και όχι της μεταφοράς του εύθραυστου νεογνού (επιβίωση 75,9%), ιδιαίτερα αν πρόκειται για νεογνό πολύ χαμηλού βάρους ή με ασυμβίβαστα με την εξωμήτριο ζωή χειρουργικά προβλήματα (εικόνα 5). Ο σκεπτικισμός των γονέων και του μαιευτήρα για την αλλαγή του τόπου τοκετού δεν θα πρέπει να είναι η αιτία να μην αντιμετωπιστεί ο μικρός ασθενής σε εξειδικευμένο κέντρο.


Συμπεράσματα
Η πορεία της περιγεννητικής αντιμετώπισης των χειρουργικών συγγενών ανωμαλιών θα πρέπει να ακολουθεί τα πιο κάτω βήματα:
1. Όταν διαπιστώνεται μία εμβρυϊκή ανωμαλία δίνεται έγκαιρα στους γονείς η δυνατότητα πρόσβασης σε εξειδικευμένη ΣΕΟ.
2. Οι γονείς πρέπει να πληροφορηθούν ότι το προγεννητικό υπερηχογράφημα τη 18η έως την 20ή εβδομάδα κύησης αναγνωρίζει μείζονες δομικές ανωμαλίες σε ποσοστό 60% των περιπτώσεων.
3. Όταν διαπιστώνεται ή πιθανολογείται μία δομική ανωμαλία πρέπει να γίνεται υπερηχογράφημα σε τριτοβάθμιο κέντρο όσο το δυνατόν συντομότερα για να βελτιωθούν οι θεραπευτικές επιλογές.
4. Σε προχωρημένες εγκυμοσύνες με εμβρυϊκές δομικές ανωμαλίες πρέπει να επαναλαμβάνεται το υπερηχογράφημα όσο συχνά απαιτείται (εξαρτάται από τον τύπο της ανωμαλίας), σε μια προσπάθεια να διαπιστωθεί η εξέλιξή τους και να διευκρινιστεί η ύπαρξη συνυπαρχουσών ανωμαλιών που πιθανόν να επηρεάσουν τις αποφάσεις της ΣΕΟ.
5. Όταν διαπιστωθεί δομική ανωμαλία στο υπερηχογράφημα 2ου επιπέδου, πιθανόν να βοηθήσουν και άλλες απεικονιστικές μέθοδοι, όπως το εμβρυϊκό υπερηχογράφημα καρδιάς, το γυναικολογικό 3-D υπερηχογράφημα, η ultrafast εμβρυϊκή MRI και επιλεκτικά ο ακτινολογικός έλεγχος και η εμβρυϊκή CT scan.
6. Ο απεικονιστικός έλεγχος των γονέων μπορεί να χρειάζεται σε περιπτώσεις όπου πιθανολογείται χρωμοσωμική νόσος.
7. Γονεϊκός και εμβρυϊκός αιματολογικός έλεγχος πιθανόν να απαιτούνται για να διευκρινιστούν διαγνωστικά ερωτήματα σε μονήρεις ή πολλές δομικές ανωμαλίες.
8. Οι γονείς πρέπει να ενημερώνονται σε ευχάριστο περιβάλλον και να διασφαλίζονται η εχεμύθεια και οι αρχές προσωπικών δεδομένων. Η αναφορά σε δομικές ανωμαλίες πρέπει να ακολουθείται από σαφείς απαντήσεις για την αντιμετώπισή τους.
9. Οι γονείς πρέπει να ενημερώνονται ότι μείζονες ή ελάσσονες δομικές ανωμαλίες μπορεί να είναι μέρος ενός γενετικού συνδρόμου, ανεξάρτητα από το εάν ο καρυότυπος είναι φυσιολογικός.
10. Εάν χρειάζεται άμεση ή επείγουσα περιγεννητική αντιμετώπιση του νεογνού για την αντιμετώπιση της ανωμαλίας, τότε ο τοκετός είναι προτιμότερο να γίνει σε κέντρο που έχει την κατάλληλη υποδομή.
11. Πρέπει να δίνονται στους γονείς οι πληροφορίες για πιθανούς αιτιολογικούς παράγοντες και για το ενδεχόμενο να παρουσιαστεί η ανωμαλία και σε επόμενες εγκυμοσύνες.
12. Σε περίπτωση διακοπής της εγκυμοσύνης, γέννησης νεκρού παιδιού ή θανάτου του νεογνού πρέπει να ενθαρρύνουμε την απόφαση νεκροψίας και παθολογοανατομικής εξέτασης για να πάρουμε το μέγιστο των πληροφοριών σχετικά με την ανωμαλία.
Τα σημαντικότερα προβλήματα στην επιλογή της καλύτερης στρατηγικής για την αντιμετώπιση των νεογνών με συγγενείς χειρουργικές ανωμαλίες είναι η ακριβής διάγνωση, η ύπαρξη συνυπαρχουσών ανωμαλιών και η σοβαρότητά τους. Η συνεργασία όλων των εμπλεκόμενων ειδικοτήτων και η βελτίωση των διαγνωστικών και θεραπευτικών μεθόδων θα δώσουν τη δυνατότητα να κερδίζουμε κάθε αγέννητο ασθενή.


Bιβλιογραφία
1. Harrison MR. Unborn: Historical perspective of the fetus as a patient. Pharos Alpha Omega Alpha Honor Med Soc. 1982; 45:19 – 24.
2. Harrison MR, Filly RA, Golbus MS. Management of the fetus with a correctable congenital defect. JAMA 1981; 246:774 – 777.
3. Langer JC, Harrison MR, Schmith KG, et al. Fetal hydrops and death from sacrococcygeal teratoma: Rationale for fetal susgery. Am J Obstet Gynecol 1989; 160:1.145 – 1.150.
4. Touloukian RJ, Hobbins JC. Maternal ultrasonography in the antenatal diafnosis of susgically correctable fetal abnormalities. J Pediatr Surg 1980; 15:373.
5. Golbus MS, Loughman WD, Epstein CJ, et al. Prenatal genetic diagnosis in 3.000 amniocentesis. N Engl J Med 1979; 300:157.
6. Hogge WA, Schonberg SA, Golbus MS. Chorionic villus sampling: Experience of the first 1.000 cases. Am J Obstet Gynecol 1986; 154:1.249.
7. Harrison MR, Golbus MS, Filly RA. The Unborn Patient: Prenatal Diagnosis and treatment, 2nd ed. Philadelphia: WB Saunders Company, 1990.
8. McCurdy CM Jr, Seeds JW. Route of delivery of infants with congenital anomalies. Clin Perinatol. 1993; 20:81 – 106.
9. Harrison MR, Adzick NS. The fetus as a patient: Surgical considerations. Ann Surg 1990; 213:279 – 291.
10. Crombleholme TM, D?Alton M, et al. Prenatal diagnosis and the pediatric surgeon: the impact of prenatal consultation on perinatal management. J Pediatr Surg. 1996; 31:156 – 62; discussion 162 – 163.
11. Raboei EH. The role of the pediatric surgeon in the perinatal multidisciplinary team. Eur J Pediatr Surg. 2008; 18:313 – 317.
12. Gagnon A, Wilson RD, Allen VM, et al. Evaluation of prenatally diagnosed structural congenital anomalies. J Obstet Gynaecol Can. 2009; 31:875 – 881, 882 – 889.
Νοέμβριος 2011